题目内容
15.${\;}_{2}^{3}$He可作为核聚变材料,以下关于${\;}_{2}^{3}$He的叙述正确的是( )| A. | ${\;}_{2}^{3}$He原子核内中子数为2 | |
| B. | ${\;}_{2}^{3}$He和${\;}_{1}^{3}$H是同一元素的不同原子 | |
| C. | ${\;}_{2}^{3}$He核外电子数为2 | |
| D. | ${\;}_{2}^{3}$He代表原子核内有2个质子和3个中子的氦原子 |
分析 元素符号的左上角数字表示质量数,左下角数字表示质子数,中子数=质量数-质子数,质子数=核外电子数;
质子数相同,中子数不同的原子互称为同位素.
解答 解:A.${\;}_{2}^{3}$He的质子数为2,质量数为3,中子数为1,故A错误;
B.${\;}_{2}^{3}$He和${\;}_{1}^{3}$H的质子数不同,分别为2、1,中子数分别为1、2,不是同一元素,故B错误;
C.${\;}_{2}^{3}$He的质子数为2,质子数=核外电子数,电子数为2,故C正确;
D.${\;}_{2}^{3}$He代表原子核内有2个质子和1个中子的氦原子,故D错误;
故选C.
点评 本题主要考查了原子符号的含义、同位素的概念,难度不大,明确概念是解答本题关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列水溶液中的电离方程式错误的是( )
| A. | Na2CO3═2Na++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | NaHCO3═Na++H++CO32- | D. | KClO3═K++Cl-+3O2- |
6.H2在Cl2中燃烧时产生苍白色的火焰.已知形成1mol H2中的化学键释放的能量为Q1KJ,破坏1mol Cl2中的化学键消耗的能量为Q2KJ,形成1mol HCl中的化学键释放的能量为Q3KJ.下列关系式中,正确的是( )
| A. | Q1+Q2<Q3 | B. | Q1+Q2<2Q3 | C. | Q1-Q2>Q3 | D. | Q1-Q2>2Q3 |
10.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.8 kJ/mol,则水电解的热化学方程式为:2H2O(l)=2H2(g)+O2(g)△H=+285.8 kJ/mol | |
| B. | 1 mol甲烷完全燃烧生成CO2和H2O(l)时放出890kJ热量,则甲烷的燃烧热化学方程式为:$\frac{1}{2}$CH4(g)+O2(g)=$\frac{1}{2}$CO2 (g)+H2O(l)△H=-445 kJ/mol | |
| C. | HF与NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ/mol | |
| D. | 由石墨比金刚石稳定可知:C(金刚石,s)=C(石墨,s)△H<0 |
20.不能用酸性KMnO4溶液鉴别的一组物质为( )
| A. | 己烷和己烯 | B. | 苯和甲苯 | C. | SO2与乙烯 | D. | 苯与苯酚溶液 |
4.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 用溴水即可鉴别苯酚溶液,2,4-己二烯和甲苯 | |
| C. | 乙酸乙酯和食用植物油均可水解生成乙醇 | |
| D. | 溴乙烷与NaOH乙醇溶液共热生成乙烯 |
5.下列现象或事实不能用同一原理解释的是( )
| A. | Cl2和H2O2都能使品红溶液褪色 | |
| B. | 漂白粉和亚硫酸钠固体长期暴露在空气中变质 | |
| C. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| D. | SO2和Na2SO3溶液都能使溴水褪色 |
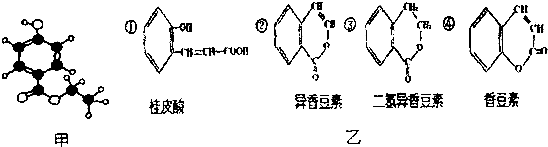
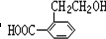
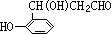 ;
;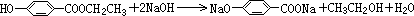 .
. (1)从不同的角度,化学反应可以有不同的分类方法,不同类别的化学反应间又有一定的联系,请在如图的方框中,用图示(每个圆圈代表一类
(1)从不同的角度,化学反应可以有不同的分类方法,不同类别的化学反应间又有一定的联系,请在如图的方框中,用图示(每个圆圈代表一类