题目内容
1.硫酸铵分解的化学方程式为 3(NH4)2SO4═4NH3↑+3X↑+N2↑+6H2O,则X的化学式为( )| A. | S | B. | O2 | C. | SO2 | D. | SO3 |
分析 反应方程式遵循质量守恒定律,根据原子守恒确定X的化学式.
解答 解:硫酸铵分解的化学方程式为:3(NH4)2SO4═4NH3↑+3X↑+N2↑+6H2O,反应遵循质量守恒定律,根据原子守恒,可知X中含有1个S原子、2个O原子,故X的化学式为SO2,故选C.
点评 本题考查化学方程式有关计算,比较基础,注意对质量守恒定律的理解应用.

练习册系列答案
相关题目
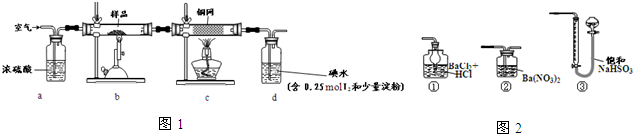
12.下列实验现象预测正确的是( )
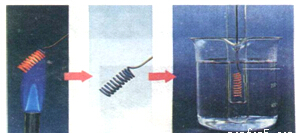
| A. |  如图实验:振荡后静置,上层溶液颜色保持不变 如图实验:振荡后静置,上层溶液颜色保持不变 | |
| B. |  如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 如图实验:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 | |
| C. |  如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 如图实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. |  如图实验IV:烧杯中先出现白色沉淀,后溶解 如图实验IV:烧杯中先出现白色沉淀,后溶解 |
16.硬水中含有较多可溶性钙、镁化合物,为降低水的硬度,下列方法可行的是( )
| A. | 煮沸 | B. | 静置 | C. | 过滤 | D. | 吸附 |
6.X、Y都是短周期元素,原子半径Y>X,它们可能形成的化合物为XY2,由此得出的正确判断是( )
| A. | X、Y可能在同一周期 | B. | X在Y的前一周期 | ||
| C. | X一定是金属元素 | D. | X一定是第三周期ⅡA或ⅣA族元素 |
13.如图所示,在用锌片、铜片和稀硫酸组成的原电池装置中,下列说法正确的是( )

| A. | 铜片上的反应为:Cu-2e-=Cu2+ | B. | 锌片上的反应为:2H++2e-=H2↑ | ||
| C. | 锌片是负极,铜片是正极 | D. | 反应一段时间后,溶液的pH变小 |
11.下列物质都具有漂白作用,其中漂白原理没有利用物质化学性质的是( )
| A. | 过氧化钠 | B. | 二氧化硫 | C. | 双氧水 | D. | 活性炭 |
 (Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家.写出乙醇燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.
(Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家.写出乙醇燃烧的化学方程式:C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.