题目内容
某中学课外兴趣小组用惰性电极电解饱和食盐水(含少量Mg2+)作系列探究,装置如图所示:
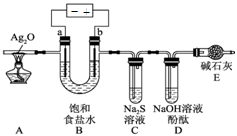
(1)电解时,甲同学发现电极a附近溶液出现浑浊,请用离子方程式表示原因:
___________________________________________________________________________________。
(2)一段时间后,你认为C中溶液可能出现的现象是_________________________________,请用离
子方程式表示原因______________________________________________________。
(3)随着反应的进行,兴趣小组的同学们都特别注意到D中溶液红色逐渐褪去。他们对溶液红色褪去主要原因提出了如下假设,请你完成假设二。
假设一:B中逸出气体与水反应生成的物质有强氧化性,使红色逐渐褪去;
假设二:______________________________________________________________________。
(4)请你设计实验验证上述假设一,写出实验步骤及结论:_____________________________________。

(1)电解时,甲同学发现电极a附近溶液出现浑浊,请用离子方程式表示原因:
___________________________________________________________________________________。
(2)一段时间后,你认为C中溶液可能出现的现象是_________________________________,请用离
子方程式表示原因______________________________________________________。
(3)随着反应的进行,兴趣小组的同学们都特别注意到D中溶液红色逐渐褪去。他们对溶液红色褪去主要原因提出了如下假设,请你完成假设二。
假设一:B中逸出气体与水反应生成的物质有强氧化性,使红色逐渐褪去;
假设二:______________________________________________________________________。
(4)请你设计实验验证上述假设一,写出实验步骤及结论:_____________________________________。
(1)2H2O+2e- = 2OH-+H2↑,Mg2++2OH-=Mg(OH)2↓(共2分,每个1分。若写成水电离、再H+得电子生成氢气和OH-与Mg2+反应生成沉淀的过程,也给分)
(2)有淡黄色沉淀(1分); Cl2+S2-=2Cl-+S↓(2分)
(3)可能是H+中和了OH-而褪色。(1分)
(4)取少量D中褪色后的溶液于试管中,加入稍过量的NaOH溶液,若不变红,则假设一正确。(2分,其它合理答案也可以)
(2)有淡黄色沉淀(1分); Cl2+S2-=2Cl-+S↓(2分)
(3)可能是H+中和了OH-而褪色。(1分)
(4)取少量D中褪色后的溶液于试管中,加入稍过量的NaOH溶液,若不变红,则假设一正确。(2分,其它合理答案也可以)
试题分析:(1)根据装置图可知,电极a与电源的负极相连,作阴极,溶液中的氢离子放电。随着氢离子的放电,a电极附近水的电离被促进,从而导致a电极负极溶液中OH-浓度增大。又因为溶液中含有镁离子,因此会产生氢氧化镁白色沉淀,有关的电极反应式为2H++2e-= H2↑、Mg2++2OH-=Mg(OH)2↓。
(2)b电极与电源的正极相连,作阳极,溶液中的氯离子放电生成氯气。氯气具有强氧化性,能把硫离子氧化生成单质S沉淀,从而使溶液变混浊,因此C中溶液可能出现的现象是有淡黄色沉淀,反应的离子方程式为Cl2+S2-==2Cl-+S↓。
(3)由于氯气溶于水生成次氯酸和盐酸,溶液显酸性,因此褪色的原因也可能是H+中和了OH-而褪色。
(4)由于次氯酸的氧化而褪色是不可逆的,即向褪色后的溶液中再滴加氢氧化钠溶液,则不会恢复用来的颜色,据此可以验证。因此正确的操作是取少量D中褪色后的溶液于试管中,加入稍过量的NaOH溶液,若不变红,则假设一正确。

练习册系列答案
相关题目
 Cu+Cl2↑
Cu+Cl2↑

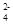 中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。
中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。