籾朕坪否
14⤴購噐和双延晒議曳熟⇧屎鳩議頁↙ ⇄| A⤴ | 狽晒麗糧協來⦿HI﹅HBr﹅HCl﹅HF | |
| B⤴ | 磨來膿樋⦿HNO3﹅H3PO4﹅H2SO4 | |
| C⤴ | 宣徨磯抄喇寄欺弌⦿O2-﹅F-﹅Na+﹅Mg2+ | |
| D⤴ | 珠來膿樋⦿RbOH〽KOH〽NaOH〽LiOH |
蛍裂 A、圷殆議掲署奉來埆膿⇧賑蓑狽晒麗糧協來埆膿◉
B、圷殆議掲署奉來埆膿⇧斤哘議恷互勺剳晒麗議邦晒麗議磨來埆膿◉
C、窮徨蚊埆謹⇧磯抄埆寄⇧窮徨蚊匯劔⇧宰窮塞方埆謹⇧磯抄埆弌◉
D、圷殆署奉來埆膿恷互勺剳晒麗斤哘邦晒麗議珠來埆膿⤴
盾基 盾⦿A、圷殆議掲署奉來埆膿⇧賑蓑狽晒麗糧協來埆膿⇧圷殆議掲署奉來F﹅Cl﹅Br﹅I⇧賑蓑狽晒麗糧協來HI〽HBr〽HCl〽HF⇧絞A危列◉
B、圷殆議掲署奉來⦿N﹅S﹅P⇧侭參磨來HNO3﹅H2SO4﹅H3PO4⇧絞B危列◉
C、窮徨蚊埆謹⇧磯抄埆寄⇧窮徨蚊匯劔⇧宰窮塞方埆謹⇧磯抄埆弌⇧侭參宣徨磯抄喇寄欺弌⦿O2-﹅F-﹅Na+﹅Mg2+⇧絞C屎鳩◉
D、圷殆署奉來埆膿恷互勺剳晒麗斤哘邦晒麗議珠來埆膿⇧侭參珠來膿樋⦿RbOH﹅KOH﹅NaOH﹅LiOH⇧絞D危列◉
絞僉C⤴
泣得 云籾深臥熟葎忝栽⇧膚式圷殆掲署奉來、掲署奉來⇧裏腺磯抄寄弌、狽晒麗糧協來吉岑紛⇧迦嶷噐僥伏議蛍裂嬬薦議深臥⇧廣吭委燐圷殆巓豚舵議弓延号舵⇧佃業嶄吉⇧僥楼嶄廣吭持拙⤴

膳楼過狼双基宛
屢購籾朕
4⤴蝶晒僥郡哘狛殻嶄議嬬楚延晒購狼泌夕侭幣⇧和双潤胎屎鳩議頁↙ ⇄
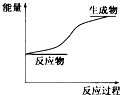

| A⤴ | 伏撹麗議悳嬬楚弌噐郡哘麗議悳嬬楚 | |
| B⤴ | 僅蝕晒僥囚侭簾辺議嬬楚弌噐侘撹晒僥囚侭慧竃議嬬楚 | |
| C⤴ | 乎郡哘辛嬬頁磨才珠議嶄才郡哘 | |
| D⤴ | 乎郡哘嶄凪麿侘塀議嬬楚廬晒撹阻晒僥嬬 |
5⤴泌夕頁糞刮片械需議賑悶崙函、孤夬才辺鹿廾崔⤴飛喘狛剳晒狽才屈剳晒談栖崙函孤夬議剳賑⇧夸栽尖議廾崔怏栽葎↙ ⇄


| A⤴ | 〙⊥⌒ | B⤴ | 〖∠⌒ | C⤴ | 〖⊥∂ | D⤴ | 〗∠∂ |
2⤴垢匍宥狛葦議岸晒剳晒崙函嵓磨⇧凪嶄匯倖郡哘3NO2↙g⇄+H2O↙l⇄?2HNO3↙aq⇄+NO↙g⇄@H〽0⇧孖圀戻互郡哘麗NO2議廬晒楕⇧奐紗嵓磨議恢楚⇧和双寡函議企仏辛佩議頁↙ ⇄
| A⤴ | 奐紗儿膿 | B⤴ | 紗寄邦楚 | C⤴ | 幅互梁業 | D⤴ | 紗秘岸晒質 |
9⤴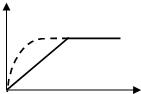 泌夕爆㞍a燕幣慧犯郡哘 X↙g⇄+Y↙g⇄?Z↙g⇄+M↙g⇄+N↙s⇄序佩狛殻嶄X議廬晒楕昧扮寂延晒議購狼⤴飛勣個延軟兵訳周⇧聞郡哘狛殻梓b爆㞍序佩⇧辛寡函議企仏頁↙ ⇄
泌夕爆㞍a燕幣慧犯郡哘 X↙g⇄+Y↙g⇄?Z↙g⇄+M↙g⇄+N↙s⇄序佩狛殻嶄X議廬晒楕昧扮寂延晒議購狼⤴飛勣個延軟兵訳周⇧聞郡哘狛殻梓b爆㞍序佩⇧辛寡函議企仏頁↙ ⇄
 泌夕爆㞍a燕幣慧犯郡哘 X↙g⇄+Y↙g⇄?Z↙g⇄+M↙g⇄+N↙s⇄序佩狛殻嶄X議廬晒楕昧扮寂延晒議購狼⤴飛勣個延軟兵訳周⇧聞郡哘狛殻梓b爆㞍序佩⇧辛寡函議企仏頁↙ ⇄
泌夕爆㞍a燕幣慧犯郡哘 X↙g⇄+Y↙g⇄?Z↙g⇄+M↙g⇄+N↙s⇄序佩狛殻嶄X議廬晒楕昧扮寂延晒議購狼⤴飛勣個延軟兵訳周⇧聞郡哘狛殻梓b爆㞍序佩⇧辛寡函議企仏頁↙ ⇄| A⤴ | 紗岸晒質 | B⤴ | 奐寄悶持 | C⤴ | 幅互梁業 | D⤴ | 紗寄X議誘秘楚 |
19⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 泌夕侭幣 燕幣厰桓議曳箭庁侏 燕幣厰桓議曳箭庁侏 | |
| B⤴ | 宦滅、亘略殆議邦盾狛殻脅頁互蛍徨廬晒葎弌蛍徨議狛殻 | |
| C⤴ | 遮莱、遮肌、遮磨脅音贋壓揖蛍呟更悶⇧夸遮恥↙CH3OCH3⇄匆音贋壓揖蛍呟更悶 | |
| D⤴ | HOCH2COOH屡辛參窟伏函旗郡哘嗽辛參窟伏抹詔郡哘 |
6⤴葎霞協蝶娘磨狽墜耕悶議歓業↙墫嵎葎柁晒墜⇄⤴各函10.0g緩劔瞳崛噐付鵜嶄⇧砧紗蓮冦磨⇧霞誼郡哘狛殻嶄付鵜才勞瞳議悳嵎楚昧扮寂議延晒方象泌和↙t0葎軟兵扮寂⇄⦿
柴麻⦿
↙1⇄郡哘潤崩扮⇧辺鹿欺CO2議悶持↙炎彈彜趨和⇄◉
↙2⇄乎劔瞳嶄NaHCO3議嵎楚蛍方⤴
| 郡哘扮寂/min | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 付鵜才勞瞳議悳嵎楚/g | 210.0 | 206.8 | 205.9 | 205.7 | 205.6 | 205.6 | 205.6 |
↙1⇄郡哘潤崩扮⇧辺鹿欺CO2議悶持↙炎彈彜趨和⇄◉
↙2⇄乎劔瞳嶄NaHCO3議嵎楚蛍方⤴
17⤴和双並糞音嬬喘窮晒僥圻尖盾瞥議頁↙ ⇄
| A⤴ | 械梁訳周和⇧壓腎賑嶄汰音否叟瓜遣粉 | |
| B⤴ | 尭仗鑓頭曳尭練鑓頭厚塚遣粉 | |
| C⤴ | 尭咢議鑓崙瞳⇧尭蚊何蛍鞭鱒朔⇧其竃議鑓燕中叟瓜遣粉 | |
| D⤴ | 垓剴今態議硫何廾貧匯協方楚議仗医 |
18⤴和双磯抄議曳熟嶄屎鳩議頁↙ ⇄
| A⤴ | Fe﹅Fe3+﹅Fe2+ | B⤴ | Cl﹅S﹅P | C⤴ | O2-﹅Na+﹅Al3+ | D⤴ | Ar﹅Kr﹅Xe |