题目内容
【题目】为分别验证温度、浓度、催化剂颗粒大小对化学反应速率的影响规律,某同学设计了如下4组实验。

(1)上表中,反应速率最快的是_______;
(2)实验3、4预期可得出的结论是_______;
(3)设计实验2、3的目的是_________;
(4)设计一个实验证明在其它条件相同时,改变温度对过氧化氢分解速率的影响(写出操作步骤)__________。
【答案】2 催化剂颗粒越小,化学反应速率越大 探究浓度对化学反应速率的影响 取相同浓度的过氧化氢溶液,控制催化剂相同,分别在不同温度下加热,观察产生气体的快慢
【解析】
(1)浓度越大反应速率越快,使用催化剂反应速率加快,催化剂颗粒越小,接触面积越大,反应速率越快;
(2)实验3、4中催化剂颗粒大小不同,探究催化剂颗粒大小对反应速率的影响;
(3)实验2、3中过氧化氢的浓度不同,探究浓度对反应速率的影响;
(4)控制其他条件相同,改变温度。
(1)其他条件相同时浓度越大、速率越快;温度越高、速率越快;催化剂可加快反应;影响程度按催化剂、温度、浓度依次减弱。温度相同,实验2的浓度最大,使用催化剂,催化剂为细颗粒,表面积较大,催化效果较好反应速率最快;
(2)实验3、4中其他条件相同,但催化剂颗粒大小不同,应是探究催化剂颗粒大小对反应速率的影响;催化剂颗粒越小,接触面积越大,反应速率越快;
(3)实验2、3中其他条件相同,只有过氧化氢的浓度不同,应是探究浓度对化学反应速率的影响;
(4)探究温度对反应速率的影响,应取相同浓度的过氧化氢溶液,控制催化剂相同,分别在不同温度下加热,观察产生气体的快慢。

【题目】分别取40mL的0.50mol·L-1盐酸与40mL的0.55mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式__。
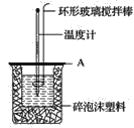
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是__。
(3)假设盐酸和NaOH溶液的密度都是1g·cm-3,又知中和后生成溶液的比热容c=4.18J·g-1·℃-1。为了计算中和热,实验时还需测量的数据有(填字母)__。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度
D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH | ||
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__。