题目内容
【题目】某城市主要空气污染物为PM2.5、SO2、NOx。科学实验小组为检测空气样本成分,用蒸馏水处理制成待测液,设计实验及所得实验现象如下:
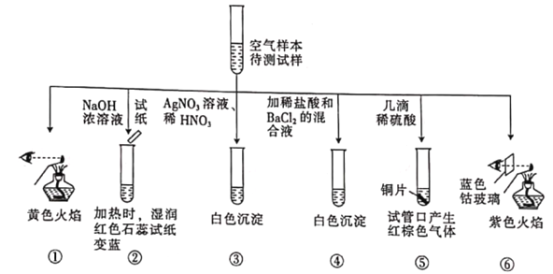
下列判断不正确的是
A. 上述实验中可用Ba(NO3)2代替BaCl2,以证明待测试样中含SO42-
B. 由实验②⑤可知待测试样中含有NH4+和NO3-
C. 焰色反应表明待测试样中含Na元素和K元素
D. 该城市的污染来源主要是燃煤和机动车尾气排放
【答案】A
【解析】
A. 酸性条件下Ba(NO3)2溶液中的硝酸根离子能将亚硫酸根离子氧化,从而干扰硫酸根离子的检验,故不能用Ba(NO3)2代替BaCl2来证明待测试样中含SO42-,选项A不正确;
B、实验②和强碱共热反应产生能使湿润红色石蕊试纸变蓝的气体,证明含有铵根离子,实验⑤溶液中加入几滴硫酸,再加入金属铜,试管口产生红棕色气体,证明原溶液含有硝酸根离子,选项B正确;
C、实验①焰色反应为黄色,所以含有钠元素,实验⑥透过蓝色钴玻璃观察焰色反应呈现紫色,证明含钾元素,故焰色反应表明待测试样中含Na元素和K元素,选项C正确;
D、根据判断可知,该城市的污染物含有硫和氮的氧化物,故主要来源是是燃煤和机动车尾气排放,选项D正确。
答案选A。

 名校课堂系列答案
名校课堂系列答案【题目】由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
B | 淀粉溶液在硫酸存在下加热一段时间后,再与新制的Cu(OH)2悬浊液混合,加热煮沸 | 无红色沉淀生成 | 淀粉没有水解 |
C | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数:Kh(CH3COO-)<Kh(HCO3-) |
D | 常温时,用两支试管各取5 mL 0.1 mol/L 酸性KMnO4溶液,分别加入0.1 mol/L和0.2 mol/L H2C2O4溶液各2 mL | 两试管溶液均褪色,且加0.2 mol/L H2C2O4溶液的试管中褪色更快 | 其它条件不变,H2C2O4溶液的浓度越大,化学反应速率越大 |
A. A B. B C. C D. D