题目内容
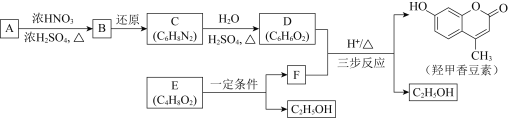
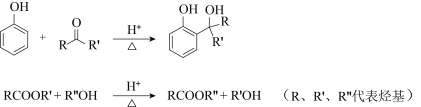
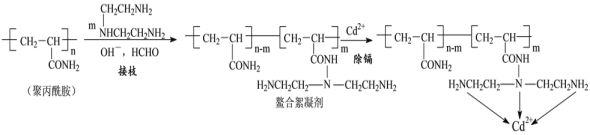
【题目】碳酸乙烯酯广泛用作电池电解质、酯类合成的中间体等。一种由CH2=CH2、CO2及O2为原料,在铁、铜及碘化物催化下的制备碳酸乙烯酯的反应如下:

(1)Fe2+基态核外电子排布式为____。
(2)写出一种与CO2互为等电子体的阴离子:____。
(3)碳酸乙烯酯中碳原子杂化轨道类型为____;1mol碳酸乙烯酯分子中含![]() 键数目为____。
键数目为____。
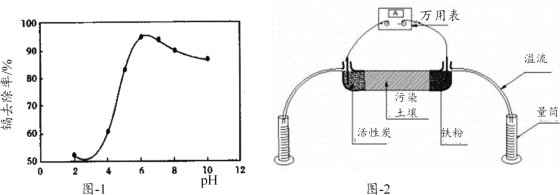
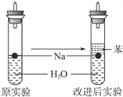
(4)FeO晶胞结构如图-1所示,晶体中与每个Fe2+紧邻的Fe2+有____个;一种由Sn、Cu、Fe及S组成的化合物的晶胞结构如图-2所示。该化合物的化学式为____。

【答案】 [Ar]3d6 或1s22s22p63s23p63d6 N3-、SCN-等 sp2和sp3 10mol或6.02×1024 12 SnCu2FeS4
【解析】(1)铁是26号元素,铁原子核外有26个电子,铁原子失去2个电子变成亚铁离子,Fe2+在基态时核外电子排布式为[Ar]3d6 或1s22s22p63s23p63d6;(2)原子数与价电子数分别等相等的是等电子体,则与CO2互为等电子体的一种离子为N3-或SCN-等;(3)碳酸乙烯酯中酯基中C原子形成3个σ键,没有孤对电子,杂化轨道数目为3,碳原子采取sp2杂化,亚甲基中C原子形成4个σ键,没有孤对电子,杂化轨道数目为4,碳原子采取sp3杂化;1mol碳酸乙烯酯中含有10mol共价键,含有的键数目为:10×6.02×1023=6.02×1024;(4)根据FeO晶胞结构可知,晶体中与每个Fe2+紧邻的Fe2+有12个;根据均摊法计算,晶胞中含Sn的个数为8×![]() =1、含Cu的个数为4×
=1、含Cu的个数为4×![]() =2、含Fe的个数为2×
=2、含Fe的个数为2×![]() =1,含S的个数为4,故该化合物的化学式为SnCu2FeS4。
=1,含S的个数为4,故该化合物的化学式为SnCu2FeS4。

【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
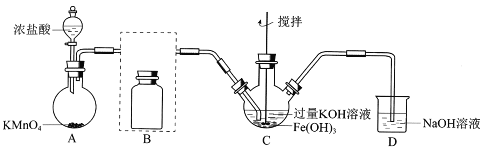
①A为氯气发生装置。A中的化学反应方程式是________________(锰被还原为Mn2+)。
②C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O,另外还有__________________(写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否为K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由____________________________________产生(用离子方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________。
②根据K2FeO4的制备实验得出:氧化性Cl2________FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。