��Ŀ����
����Ŀ���ӣ�Cd����һ����;�㷺�Ľ�����Ҳ�Ƕ����彡����в�����к�Ԫ��֮һ��
��1��1.00gCdS������ȫȼ������CdO�����SO2����ų�2.75kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ____��
��2�������£�Ksp(CdCO3) = 4.0��10��12��Ksp[Cd(OH)2] = 3.2 ��10��14�����ܽ�ȣ�mol��L��1���ϴ����____ [�CdCO3����Cd(OH)2��]������112mg��L��1 Cd2+�ķ�ˮ�Ӽ��pH��9.0���ﵽƽ��ʱ����Һ��c(Cd2+)=____��
��3��һ���������������Ʊ���������ȥ�����ӷ�ˮ��Cd2+��ԭ�����£�

�پ۱������ĵ���Ľṹ��ʽΪ____��
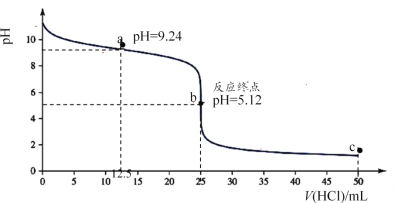
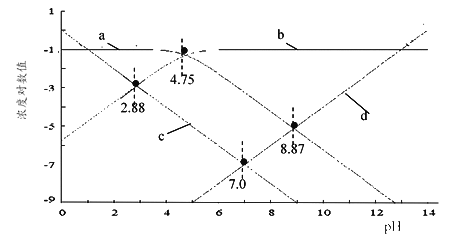
��ʹ����������������ij���ӷ�ˮ����ȥ������pH�Ĺ�ϵ��ͼ-1��ʾ����ǿ���������£�pHԽС����Ч��Խ���ԭ����____��

��4��һ���õ綯��ѧ��������Ⱦ��������װ����ͼ-2��ʾ��
��ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ���Ŀ����____��
��ʵ������������Ϸ����ĵ缫��ӦΪ____��
�ۻ���̿��������____��
���𰸡� 2CdS(s) + 3O2(g) = 2CdO(s) +2SO2(g) ��H =��792kJ��mol��1 Cd(OH)2 3.2��10��4 mol��L��1 CH2=CHCONH2 H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��� ��ȥ���۱������ۺ����� Fe ��2e��= Fe2+ ���������������Ǩ�����ü���Χ��Cd2+��������
����������1��1.00gCdS������ȫȼ������CdO�����SO2����ų�2.75kJ��������288g��2mol CdS������ȫȼ������CdO�����SO2����ų�2.75��288kJ=792kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ2CdS(s) + 3O2(g) = 2CdO(s) +2SO2(g) ��H =��792kJ��mol��1����2����ΪCdCO3��Cd(OH)2 ����ͬһ��������,ǰ��ΪAB��,����ΪAB2��.���Բ���ֱ�ӱȽ�Ksp����Ҫ��������Һ�е��ܽ��s(mol / L)�� CdCO3 ���ܽ��s =![]() = 2.0��10-6 (mol/L) �� Cd(OH)2 ���ܽ��s =
= 2.0��10-6 (mol/L) �� Cd(OH)2 ���ܽ��s = ![]() = 2 ��10-5 (mol/L)�������ܽ�ȣ�mol��L��1���ϴ����Cd(OH)2�������£�pH=9.0��c(OH-)=10-5mol/L��Ksp[Cd(OH)2] = c(Cd2+)c2(OH-)= c(Cd2+)����10-5mol/L��2= 3.2 ��10��14��c(Cd2+)= 3.2��10��4 mol��L��1����3���پ۱������ĵ���Ϊ����������ṹ��ʽΪCH2=CHCONH2����H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��ԣ�����ǿ���������£�pHԽС����Ч��Խ���4����ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ��Գ�ȥ���۱������ۺ����⣻��ʵ�������������Ϊԭ��صĸ�������������ʧ���Ӳ����������ӣ��ʷ����ĵ缫��ӦΪFe ��2e��= Fe2+���ۻ���̿�����������������������Ǩ�����ü���Χ��Cd2+�������ӡ�
= 2 ��10-5 (mol/L)�������ܽ�ȣ�mol��L��1���ϴ����Cd(OH)2�������£�pH=9.0��c(OH-)=10-5mol/L��Ksp[Cd(OH)2] = c(Cd2+)c2(OH-)= c(Cd2+)����10-5mol/L��2= 3.2 ��10��14��c(Cd2+)= 3.2��10��4 mol��L��1����3���پ۱������ĵ���Ϊ����������ṹ��ʽΪCH2=CHCONH2����H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��ԣ�����ǿ���������£�pHԽС����Ч��Խ���4����ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ��Գ�ȥ���۱������ۺ����⣻��ʵ�������������Ϊԭ��صĸ�������������ʧ���Ӳ����������ӣ��ʷ����ĵ缫��ӦΪFe ��2e��= Fe2+���ۻ���̿�����������������������Ǩ�����ü���Χ��Cd2+�������ӡ�

 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�