题目内容
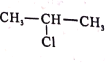
【题目】某溶液 只含Cl-、![]() 、SO4 2-、Na+、K+、Mg2+六种离子中的某几种。经实验:
、SO4 2-、Na+、K+、Mg2+六种离子中的某几种。经实验:
①原溶液加过量的 NaOH 溶液,产生白色沉淀;
②过滤,取实验①滤液加 BaCl2 溶液不产生沉淀;
③取实验①滤液加稀硝酸酸化,再加 AgNO3 溶液产生白色沉淀, 下列说法不正确的是
A.实验 ① 中的白色沉淀为 Mg(OH)2
B.实验②证明原溶液中一定没有 CO3 2-、SO4 2-
C.原溶液中一定含有的离子是 Cl-、Na+、K+、Mg2+
D.有同学认为原溶液一定有 Cl-,实验③可以省略
【答案】C
【解析】
①溶液中加入过量NaOH生成白色沉淀,该沉淀应为Mg(OH)2,说明溶液中含有Mg2+,则不含有CO32-;②过滤,取实验①滤液加 BaCl2 溶液不产生沉淀,说明溶液中不含SO42-;③取实验①滤液加稀硝酸酸化,再加 AgNO3 溶液产生白色沉淀, 说明含有Cl-,据此分析解题。
①溶液中加入过量NaOH生成白色沉淀,该沉淀应为Mg(OH)2,说明溶液中含有Mg2+,则不含有CO32-;②过滤,取实验①滤液加 BaCl2 溶液不产生沉淀,说明溶液中不含SO42-;③取实验①滤液加稀硝酸酸化,再加 AgNO3 溶液产生白色沉淀, 说明含有Cl-;
A.由分析知:实验① 中的白色沉淀为 Mg(OH)2,故A正确;
B.由分析知:实验②证明原溶液中一定没有 CO3 2-、SO4 2-,故B正确;
C.由分析知:原溶液中一定含有的离子是Cl-和Mg2+,可能含有的离子是Na+、K+,故C错误;
D.由实验①溶液中一定含有Mg2+,实验②溶液中一定没有 CO3 2-、SO4 2-,结合溶液是电中性的,则溶液中一定含有Cl-,实验③可以省略,故D正确;
故答案为C。

练习册系列答案
相关题目