题目内容
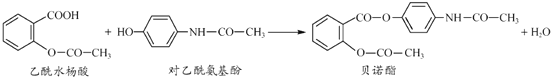
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得,下列有关叙述正确的是( )
A. 根据有机物的分类,贝诺酯属于芳香烃,分子式为![]()
B. 乙酰水杨酸和对乙酰氨基酚均能与![]() 溶液反应放出
溶液反应放出![]()
C. 乙酰水杨酸和对乙酰氨基酚可用![]() 溶液区别
溶液区别
D. 1mol乙酰水杨酸最多能与2molNaOH发生反应
【答案】C
【解析】
A.贝诺酯含有氧元素,而烃只含C、H元素,选项A错误;
B.对乙酰氨基酚与碳酸钠反应生成碳酸氢钠,不能生成二氧化碳,选项B错误;
C.对乙酰氨基酚含有酚羟基,具有酚类的性质,可与氯化铁溶液发生显色反应,可鉴别,选项C正确;
D.乙酰水杨酸水解产物共含有2个羧基、1个酚羟基,则1mol乙酰水杨酸最多能与3molNaOH发生反应,选项D错误。
答案选C。

练习册系列答案
相关题目
【题目】下列实验操作能达到实验目的的是( )
实验目的 | 实验操作 | |
A | 制备 | 将 |
B | 由 | 将 |
C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
D | 配制 | 将氯化铁固体溶于盐酸中 |
A. AB. BC. CD. D

