题目内容
12.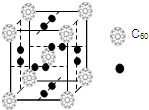 科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
分析 根据晶胞的分配原则计算出每个晶胞结构各离子的个数,在晶胞中,每个面上有两个钾原子,每个顶点上和体心有一个C60.
解答 解:在晶胞中,每个面上有两个钾原子,每个顶点上和体心有一个C60,根据均摊法可知K原子个数为6×2×$\frac{1}{2}$=6,C60分子的个数比为8×$\frac{1}{8}$+1=2;所以K原子个数为和C60分子的个数比为6:2=3:1,
故答案为:3:1.
点评 本题考查了均摊法在晶胞计算中的应用,题目难度不大,注意把握微粒在晶胞中的位置以及在晶胞中所占比例为解题的关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
3.下列说法正确的是( )
| A. | 制氧气时,用Na2O2或H2O2作反应物应该选择不同的气体发生装置 | |
| B. | 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| C. | 侯氏制碱法的工艺过程中应用了物质溶解度的差异 | |
| D. | 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀时的离子方程式为:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
7.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答下列问题:
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱若a=7,HA为强酸;若a>7,HA为弱酸.
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol/L否(填“是”或“否”).混合溶液中离子浓度c(A-)与c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中c(A-)+c(HA)=c(Na+)或0.05mol/L.
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱若a=7,HA为强酸;若a>7,HA为弱酸.
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol/L否(填“是”或“否”).混合溶液中离子浓度c(A-)与c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中c(A-)+c(HA)=c(Na+)或0.05mol/L.
17.下列叙述中,正确的是( )
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) $?_{500℃/30MPa}^{催化剂}$2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| D. | 含 1mol NaOH的稀溶液分别和含1mol CH3COOH、1mol HNO3的稀溶液反应,后者比前者放出的热量多 |
4.下列应用不涉及氧化还原反应的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | 工业上电解熔融状态Al2O3制备Al | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 实验室用NH4Cl 和Ca(OH)2制备NH3 |
1.下列说法不正确的是( )
| A. | D和T互为同位素 | B. | C2H6和CH3CH2CH2CH3互为同系物 | ||
| C. | C.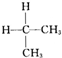 与 与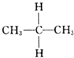 互为同分异构体 互为同分异构体 | D. | O2和O3互为同素异形体 |
2.某工厂排放的工业废水中可能含有K+、Al3+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子.经检测废水呈明显的碱性,则可确定该厂废水中肯定不大量含有的离子组合是( )
| A. | Al3+、NH4+、Mg2+、HCO3- | B. | K+、NH4+、NO3-、SO42- | ||
| C. | Al3+、K+、NO3-、HCO3- | D. | K+、Mg2+、SO42-、Cl- |