题目内容
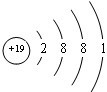
12.微粒甲与离子乙在溶液中的转化关系如下所示:微粒甲$\stackrel{OH-}{→}$离子乙$\stackrel{H+}{→}$微粒甲,则微粒甲是( )| A. | Al2O3 | B. | NH4+ | C. | Fe3+ | D. | CO2 |
分析 根据微粒甲能与氢氧根反应生成乙,乙能与氢离子反应再生成甲解题,将选项带入转化关系,符合即可.
解答 解:A.Al2O3与氢氧根能反应生成AlO2-,与氢离子反应生成沉淀或铝离子,得不到Al2O3,不符合转化关系,故A错误;
B.NH4+与OH-反应生成NH3•H2O,NH3•H2O不是离子,不符合转化关系,故B错误;
C.Fe3+与OH-反应生成Fe(OH)3,不是离子,不符合转化关系,故C错误;
D.CO2与氢氧根能反应生成碳酸根离子,碳酸根离子和氢离子反应生成水和CO2,故D正确.
故选D.
点评 本题考查无机物的推断,为高频考点,把握物质的性质及图中转化关系为解答的关键,注意A、B为易错点,把握物质的性质,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.可以将五种无色液体:乙醇、溴乙烷、KI溶液,苯酚溶液,甲苯一一区分开的试剂( )
| A. | Fe(NO3)2溶液 | B. | 溴水 | C. | 酸性KMnO4溶液 | D. | NaOH溶液 |
7.在恒容密闭容器中,充入2mol SO2和2mol O2,发生反应:2SO2(g)+O2(g)═2SO3(g)△H<0
反应达到平衡后,下列措施能使正反应速率加快,且c(SO3)增大的是( )
反应达到平衡后,下列措施能使正反应速率加快,且c(SO3)增大的是( )
| A. | 升高温度 | B. | 加入适当的催化剂 | ||
| C. | 充入He(g),使体系压强增大 | D. | 再向容器中通入2molO2 |
2.根据相关化学概念和原理,下列判断正确的是( )
| A. | 若某反应的生成物总能量低于反应物总能量,则该反应为吸热反应 | |
| B. | 若将反应Fe+2Fe3+=3Fe2+设计成原电池,则正极材料一定为铁 | |
| C. | 若R2+和M+的电子层结构相同,则原子序数:R>M | |
| D. | 若甲、乙两种有机物具有相同的分子式,不同的结构,则甲和乙一定是同分异构体 |

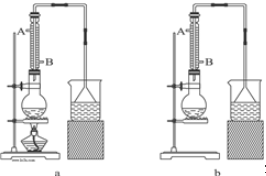 (2)冷凝管中的冷凝水的流向应是B
(2)冷凝管中的冷凝水的流向应是B