题目内容
4.溴乙烷是有机合成的重要原料.农业上用作仓储谷物、仓库及房舍等的熏蒸杀虫剂;也常用于汽油的乙基化、冷冻剂和麻醉剂.实验室用NaBr、浓H2SO4、乙醇为原料,制备溴乙烷,反应的化学方程式为:已知反应物的用量:0.3mol NaBr(s);0.25mol乙醇;36mL浓硫酸(溶质质量分数为98%,密度为1.84g/mL);25mL水,其中乙醇的密度为0.80g/mL.回答下列问题:
(1)该实验应选择下图中的a(填“a”或“b”)装置.
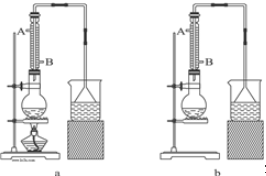 (2)冷凝管中的冷凝水的流向应是B
(2)冷凝管中的冷凝水的流向应是BA.A进B出 B.B进A出 C.从A进或B进均可
(3)上述实验完成后,需要将烧瓶中的有机物蒸馏出来,所得馏出液中含有CH3CH2Br、CH3CH2OCH2CH3.
(4)用棕黄色的粗溴乙烷制取无色的溴乙烷应加入的试剂是NaOH溶液,必须使用的仪器是分液漏斗.
(5)本实验的产率为60%,则可制取溴乙烷16.35g.
(6)为除去溴乙烷中残留的少量水,可选用无水CaCl2作干燥剂,并蒸馏.为证明最终得到的产品--溴乙烷中含有溴元素,可采取的实验方法是将溴乙烷和氢氧化钠溶液混合共热,所的产物用硝酸酸化后,再加入硝酸银溶液后,若有浅黄色沉淀则证明含有溴元素.
分析 (1)该反应需要加热,根据a、b装置的不同点进行解答;
(2)从冷凝的原理来解答;
(3)根据发生的反应和副反应判断;
(4)粗溴乙烷中含有单质溴,可以用氢氧化钠除去,然后分液;
(5)n(乙醇)=0.25mol,然后根据产率的概念来解答;
(6)检验溴乙烷中溴元素,应先在碱性条件下水解,然后加入硝酸酸化,最后加入硝酸银,观察是否有淡黄色沉淀生成,如果有淡黄色沉淀生成说明溴乙烷中含有溴元素.
解答 解:(1)由题给信息,知该反应为:NaBr+H2SO4+C2H5OH$\stackrel{△}{→}$NaHSO4+C2H5Br+H2O,反应需要加热,所以应采用装置a,
故答案为:a;
(2)冷凝时,水需充满冷凝器,为了防止冷凝器冷凝时,受热不均匀破裂,冷凝水应下进上出.故答案为:B;
(3)实验中发生的反应为C2H5-OH+HBr$→_{△}^{浓硫酸}$C2H5Br+H2O,2C2H5OH $→_{140℃}^{浓硫酸}$C2H5OC2H5+H2O,则将烧瓶中的有机物蒸馏出来,所得馏出液中含有CH3CH2Br、CH3CH2OCH2CH3;
故答案为:CH3CH2Br、CH3CH2OCH2CH3;
(4)粗溴乙烷中含有单质溴,可以加NaOH溶液,NaOH与溴单质反应生成溴化钠和次溴酸钠水溶液,然后分液,分液时用到的分液漏斗;
故答案为:NaOH溶液;分液漏斗;
(5)n(乙醇)=0.25mol,实验的产率为60%,则n(溴乙烷)=0.25mol×60%=0.15mol,m(溴乙烷)=0.15mol×109g/mol=16.35g,
故答案为:16.35;
(6)检验溴代烃中含有溴元素首先将它转化为溴离子,采用溴代烃的水解方法,即加入氢氧化钠,然后加入硝酸酸化,水解后生成的溴离子可以和银离子反应,生成淡黄色不溶于硝酸的沉淀溴化银,由此来检验溴乙烷中的溴元素,所以操作为:将溴乙烷和氢氧化钠溶液混合共热,所的产物用硝酸酸化后,再加入硝酸银溶液后,若有浅黄色沉淀则证明含有溴元素;
故答案为:将溴乙烷和氢氧化钠溶液混合共热,所的产物用硝酸酸化后,再加入硝酸银溶液后,若有浅黄色沉淀则证明含有溴元素.
点评 该题较为综合,主要考查了溴乙烷的制备,掌握相关物质的基本化学性质,是解答本题的关键,平时须注意积累相关反应知识,难度中等.

| A. | 属于烃类物质 | B. | 相对分子质量为46 | ||
| C. | 分子中含有的官能团是羟基 | D. | 在空气中完全燃烧生成CO2和H2O |
| A. | Al2O3 | B. | NH4+ | C. | Fe3+ | D. | CO2 |
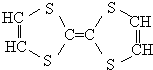 用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )
用于制造隐形飞机的物质具有吸收微波的功能,其主要成分的结构如图,关于该分子的说法正确的有( )| A. | 分子中含有碳碳双键,属于烯烃 | |
| B. | 从碳骨架形状分析,应该属于环状烃 | |
| C. | 该分子属于高分子化合物 | |
| D. | 该分子中即有极性键,也有非极性键 |
| A | B | ||
| C | D | E |
(2)B的气态氢化物与其最高价氧化物对应水化物可形成盐,其盐溶液显酸性(填“酸性”、“中性”或“碱性”)用离子方程式表示其原因:NH4++H2O?NH3.H2O+H+.
(3)写出C元素原子的价电子排布式:3s23p1比较B、E元素基态原子的第一电离能大小N>S(用元素符号填空).
(4)A与氢元素形成最简单化合物H可作为燃料电池的原料,写出该燃料电池(以足量NaOH溶液作为电解质溶液)负极电极反应CH4+10 OH--8e-=CO32-+7H2O已知25℃/101kPa下,H的燃烧热为890kJ•mol-1,写出H燃烧热的化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ•mol-1.
(5)向150ml.0.10•L-1的氯化物溶液中加入40mLNaOH溶掖,充分反应后得到0.78g沉淀.则原NaOH溶液的物质的量浓度可能是0.75或1.5mol•L-1.
| A. | Ag+ NH3 | B. | Cu2+ NH3 | C. | H+ H2O | D. | Ag+ CH4 |
| A. | 固体小颗粒 | B. | SO2 | C. | 氮氧化物 | D. | CO2 |