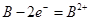题目内容
下列关于下图装置的说法正确的是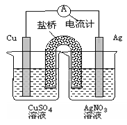
| A.银电极是负极 |
| B.铜电极上发生的反应为Cu-2e-=Cu2+ |
| C.外电路中的电子是从银电极流向铜电极。 |
| D.该装置能将电能转化为化学能 |
B
解析试题分析:Cu与Ag相比更活泼,因此在左图装置中Cu失去电子形成Cu2+,Ag+得到电子形成Ag。在Cu电极上发生的反应为Cu-2e-=Cu2+,在Ag电极上发生的反应为Ag++ e-=Ag,外电路中的电子是从铜电极流向银电极,C错误。银电极得到电子为正极,A错误。整个装置没有电源,是将化学能转换为电能,D错误。
考点:原电池的基本原理

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
下列有关金属腐蚀与防护的说法中正确的是
| A.在生产生活中比较普遍而且危害较大的是金属的化学腐蚀 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
某小组为研究电化学原理,设计如图装置。下列叙述错误的是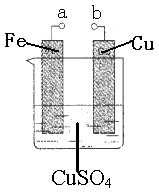
| A.a和b不连接时,铁片质量会增加 |
| B.a和b用导线连接时,正极发生的电极反应为:Cu2++2e-=Cu |
| C.无论a和b是否连接,铁片均被腐蚀 |
| D.a和b分别连接电源正、负极时,Fe电极发生的电极反应为:4OH--4e-=2H2O+O2↑ |
用惰性电极电解CuSO4溶液一段时间后,停止电解,向所得溶液中加入0.1 mol Cu(OH)2,溶液浓度恢复至电解前。关于该电解过程的说法不正确的是
| A.生成Cu的物质的量是0.1 mol |
| B.转移电子的物质的量是0.2 mol |
| C.随着电解的进行溶液的pH减小 |
| D.阳极反应式是4OH--4e-=2H2O+O2↑ |
如图是一种染料敏化太阳能电池的示意图。电池的一个电极由有机光敏燃料(S)涂覆在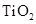 纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:
纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为: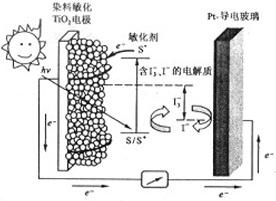
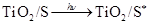 (激发态)
(激发态)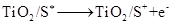
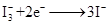
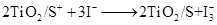
下列关于该电池叙述错误的是:
| A.电池工作时,是将太阳能转化为电能 |
| B.电池工作时,I-离子在镀铂导电玻璃电极上放电 |
| C.电池中镀铂导电玻璃为正极 |
| D.电池的电解质溶液中I-和I3-的浓度不会减少 |
下列叙述中错误的是
| A.电解池是电能转化为化学能的装置 |
| B.原电池跟电解池链接后,电子从原电池负极流向电解池阳极 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.用惰性电极电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气 |
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:电池 Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l)
电解池 2Al + 3H2O = Al2O3 + 3H2,对该电解过程,以下判断正确的是
| | 电池 | 电解池 |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成1molAl2O3 |
| C | 正极:PbO2+4H++2e—=Pb2++2H2O | 阳极:2Al+3H2O—6e—=Al2O3+6H+ |
| D | Pb电极反应质量不变 | Pb电极反应质量不变 |
下列说法中正确的是
| A.在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率 |
| B.粗铜精炼时,电镀液中的c(Cu2+)保持不变 |
| C.纯银在空气中久置变黑发生的是电化学腐蚀 |
| D.阴极电保护法是将被保护的金属与外加电源的正极相连 |
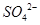 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是