题目内容
把Fe和Fe2O3组成的某混合物放入250mL2.0mol·L-1的HNO3溶液中,充分反应后,生成的NO气体在标准状况下的体积为1.12L,再向反应后的溶液中加入1.0mol·L-1的NaOH溶液,要使铁元素完全沉淀下来,所加入的NaOH溶液的体积最少是( )
| A.400mL | B.450mL | C.500mL | D.550mL |
B
正确答案:B
Fe2+和Fe3+都是和NO3-配合,反应后NO3-的量为 0.25×2 -1.12/22.4=0.45 mol,加NaOH 相当于把剩下的NO3-换成OH-,因此NaOH 需要 0.45 mol 即 450ml。

练习册系列答案
相关题目
 列问题:
列问题:

 (2)碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的方程式为:KI + 3H2O KIO3 + 3H2↑。则阳极材料为 。
(2)碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的方程式为:KI + 3H2O KIO3 + 3H2↑。则阳极材料为 。 K2SO4+ I2+ H2O
K2SO4+ I2+ H2O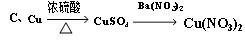
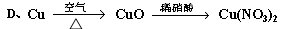
 学方程式为 ;
学方程式为 ;
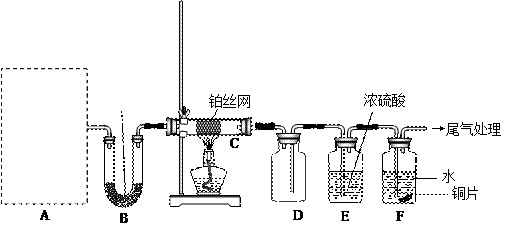
 检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。