题目内容
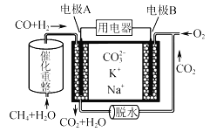
【题目】某熔融碳酸盐燃料电池原理示意如图,下列有关该电池的说法正确的是
A. CH4+H2O![]() 3H2+CO,1molH2O参加反应转移12×6.02×1023个电子
3H2+CO,1molH2O参加反应转移12×6.02×1023个电子
B. 电极A为正极
C. CH4在电极上被氧化
D. 电池工作时,CO32-向电极A移动
【答案】D
【解析】
仔细观察熔融碳酸盐燃料电池原理示意图,分析物质的转化过程中元素化合价的变化,结合原电池工作原理作答。
A.分析反应CH4+H2O![]() 3H2+CO化合价的升降知,CH4和H2O分子中1个氢原子化合价都由+1价降到0价,每个氢原子得1e-。1molCH4和1molH2O中共有氢原子6mol,共转移6×6.02×1023个电子,所以1molH2O参加反应转移6×6.02×1023个电子,A项错误;
3H2+CO化合价的升降知,CH4和H2O分子中1个氢原子化合价都由+1价降到0价,每个氢原子得1e-。1molCH4和1molH2O中共有氢原子6mol,共转移6×6.02×1023个电子,所以1molH2O参加反应转移6×6.02×1023个电子,A项错误;
B.观察熔融碳酸盐燃料电池原理示意图可知,电极A通入CO和H2,放电后产物是CO2和H2O,CO中的碳元素由+2价升高到+4价,H2中氢元素由0价升高到+1价,由此可知电极A上失去电子,发生氧化反应,所以电极A是负极,A项错误;
C.从熔融碳酸盐燃料电池原理示意图看出,CH4和H2O先进行催化重整,产生CO和H2,CO和H2再通入电极A,所以CH4并没有直接参与电极反应,C项错误;
D.燃料电池工作即放电时属于原电池反应,原电池的电解质溶液中阴离子向负极移动,由B项分析知电极A是负极,所以CO32-向电极A移动,D项正确;答案选D。

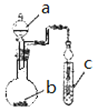
【题目】利用图示装置进行下列实验,能达到实验目的的是
溶液a | 固体b | 溶液c | 实验目的:验证 |
| |
A | 浓硝酸 | NaHCO3 | Na2SiO3 | 非金属性:N>C>Si | |
B | 浓盐酸 | KMnO4 | Na2S | 氧化性:KMnO4>Cl2>S | |
C | 浓盐酸 | CaCO3 | NaAlO2 | 酸性:HCl>H2CO3>Al(OH)3 | |
D | 浓氨水 | CaO | 酚酞溶液 | NH3·H2O是弱碱 |
A. A B. B C. C D. D