题目内容
16. 甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 金属性:甲>乙>丁 原子半径:己>辛>戊 | |
| B. | 辛是金属元素,元素符号为Ge | |
| C. | 丙与庚的原子核外电子数相差13 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物. |
分析 戊的一种单质是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲为Li,可推知乙为Na、丙为K、丁为Ca、己为Si、庚为Ge、辛为Ga.
A.同主族从上到下金属性增强,根据金属活动顺序表判断钠与Ca的金属性强弱;同周期自左而右原子半径减小,同主族自上而下原子半径增大;
B.辛为Ga元素;
C.丙处于第四周期第1列,庚处于第四周期第14列,第四周期每一列容纳一种元素;
D.钠在空气中燃烧生成过氧化钠.
解答 解:戊的一种单质是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲为Li,可推知乙为Na、丙为K、丁为Ca、己为Si、庚为Ge、辛为Ga.
A.同主族从上到下金属性增强,由金属活动顺序表可知Ca的金属性比Na强,则金属性:甲<乙<丁;同周期自左而右原子半径减小,同主族自上而下原子半径增大,则原子半径为:辛>己>戊,故A错误;
B.辛为Ga元素,故B错误;
C.丙处于第四周期第1列,庚处于第四周期第14列,第四周期每一列容纳一种元素,故二者原子序数相差13,故C正确;
D.钠在空气中燃烧生成过氧化钠,过氧化钠含有离子键、共价键,故D错误,
故选C.
点评 本题考查位置结构性质的关系,难度中等,关键是根据金刚石的硬度及甲与戊的原子序数关系推断各元素为解答的关键,A选项中注意根据金属活动顺序表判断Ca的金属性比Na强.

练习册系列答案
相关题目
6.已知:CH4+Br2$\stackrel{光}{→}$CH3Br+HBr;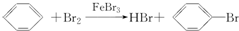
将甲苯与液溴混合,加入铁粉,其反应产物可能有( )
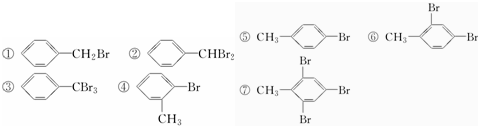
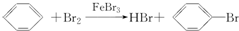
将甲苯与液溴混合,加入铁粉,其反应产物可能有( )

| A. | 只有①②③ | B. | 只有④⑤⑥⑦ | C. | 只有①⑤ | D. | ①②③④⑤⑥⑦ |
7.向100mL 18mol/L H2SO4溶液中加入足量的铜片并加热.充分反应后,则的参加反应H2SO4的物质的量( )
| A. | 小于1.8mol | B. | 等于0.9mol | C. | 等于1.8mol | D. | 大于1.8mol |
4.下列混合物可用加热的方法分离的是( )
| A. | 碘和氯化铵 | B. | 硫酸钾和氯酸钾 | ||
| C. | 氯化铵和硫酸钡 | D. | 碳酸氢钠和碳酸氢铵 |
11.下表是元素周期表的一部分,表中序号分别代表某一元素.请回答下列问题.
(1)①-⑩中,最活泼的金属元素是Na(写元素符号,下同);最不活泼的元素是Ar;可作半导体材料的元素是Si;某元素的气态氢化物与其最高价氧化物的水化物可直接化合生成一种盐,该元素是N.
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)元素的非金属性:①>⑦(填“>”或“<”).
(5)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);
碱性最强的是NaOH(填化学式),它与⑥的最高价氧化物的水化物反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)元素的非金属性:①>⑦(填“>”或“<”).
(5)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);
碱性最强的是NaOH(填化学式),它与⑥的最高价氧化物的水化物反应的离子方程式为OH-+Al(OH)3=AlO2-+2H2O.
1.下列属于纯净物的是( )
| A. | 汽油 | B. | 煤 | C. | 乙烯 | D. | 石油裂解气 |
8.下列事实,不能说明氯元素的非金属性比硫元素强的是( )
| A. | 盐酸是强酸,氢硫酸是弱酸 | B. | HClO4酸性比H2SO4强 | ||
| C. | 氯气与H2S能发生置换反应 | D. | 受热时,氯化氢比硫化氢稳定 |
5.将铜片和石墨棒用导线相连(其间连有电流表),并同时插入Fe2(SO4)3溶液中,下列现象中不可能出现的是( )
| A. | 铜片质量减少 | B. | 石墨棒质量增加 | C. | 电流表指针偏转 | D. | 溶液显蓝色 |
6.常温下,将0.2mol•L-1 CH3COOK 与0.1mol•L-1盐酸等体积混合后,溶液的pH<7,则溶液中下列微粒的物质的量浓度的关系正确的是( )
| A. | c(CH3COO-)=c(Cl-)=c(H+)>c(CH3COOH) | B. | c(CH3COO-)=c(Cl-)>c(CH3COOH)>c(H+) | ||
| C. | c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | D. | c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |