题目内容
6.某澄清透明溶液可能由Na+、Cu2+、Ba2+、CO32-、SO42-、Cl-等若干种离子组成.取溶液进行如下实验①用PH试纸检验,该溶液的PH>7
②取适量试液,加入过量盐酸,有气体生成,并得到溶液
③在②所得溶液中加入过量氢氧化钡溶液,产生白色沉淀甲,过滤
④在③中所得的滤液中加入稀硝酸酸化,再加入硝酸银溶液,产生白色沉淀
根据上述实验回答下列问题
(1)原溶液中一定不存在的离子是Cu2+、Ba2+
(2)原溶液中一定存在的离子是Na+、CO32-
(3)原溶液中可能存在的离子是SO42-、Cl-.
分析 ①用PH试纸检验,该溶液的PH>7,说明呈碱性,为强酸弱碱盐,应含有CO32-,则不含Cu2+、Ba2+;
②取适量试液,加入过量盐酸,有气体生成,应生成二氧化碳;
③在②所得溶液中加入过量氢氧化钡溶液,产生白色沉淀甲,应为碳酸钡,可能含有硫酸钡;
④在③中所得的滤液中加入稀硝酸酸化,再加入硝酸银溶液,产生白色沉淀,生成AgCl沉淀,但不能确定是否含有Cl-.
解答 解:①用PH试纸检验,该溶液的PH>7,说明呈碱性,为强酸弱碱盐,应含有CO32-,则不含Cu2+、Ba2+,由溶液的电中性可知一定含有Na+,
②取适量试液,加入过量盐酸,有气体生成,应生成二氧化碳;
③在②所得溶液中加入过量氢氧化钡溶液,产生白色沉淀甲,应为碳酸钡,可能含有硫酸钡;
④在③中所得的滤液中加入稀硝酸酸化,再加入硝酸银溶液,产生白色沉淀,生成AgCl沉淀,由于②加入盐酸,则不能确定是否含有Cl-.
由以上分析可知一定含有Na+、CO32-,一定不存在Cu2+、Ba2+,可能存在的离子有SO42-、Cl-,
故答案为:(1)Cu2+、Ba2+;(2)Na+、CO32-;(3)SO42-、Cl-.
点评 本题考查了常见离子的检验方法,题目难度不大,注意根据溶液呈电中性判断溶液中存在的离子方法,本题充分考查了学生的分析、理解能力,要求熟练掌握常见离子的检验方法.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
17.常温下pH=9的Ca(OH)2溶液与pH=13的NaOH溶液按体积比4:1混合,溶液中氢离子的浓度(mol/L)为( )
| A. | 5.0×10-13 | B. | 2.0×10-12 | ||
| C. | $\frac{1}{5}$(1×10-+4×10-5) | D. | $\frac{1}{5}$(1×10-13+4×10-9) |
14.已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6KJ/mol有关键能数据如下表:
则水分子中O-H键键能为( )
| 化学键 | H-H | O=O |
| 键能/KJ?mol-1 | 436 | 498 |
| A. | 463.4KJ/mol | B. | 926.8KJ/mol | C. | 221.6KJ/mol | D. | 413KJ/mol |
1.对于下列事实的解释错误的是( )
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 氯水可使石蕊试液先变红后褪色,说明氯水具有酸性、漂白性 |
11.下列有关焰色反应实验操作的说明不正确的是( )
| A. | 没有铂丝可用无锈铁丝代替 | |
| B. | 先灼烧铂丝直到与酒精灯火焰颜色相同时,再蘸被检物质 | |
| C. | 再做不同金属的焰色反应时都要将铂丝蘸取氢氧化钠溶液洗涤并灼烧至没有颜色 | |
| D. | 焰色反应可以用于某些金属离子的鉴别 |
18.下列叙述正确的为( )
| A. | 石墨转化为金刚石属于化学变化 | |
| B. | 金刚石和石墨具有相似的物理性质 | |
| C. | C60是碳元素的一种单质,其摩尔质量为720 | |
| D. | 由碳元素单质组成的物质一定是纯净物 |
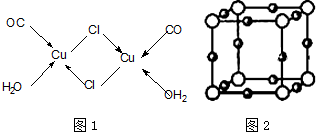
 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.
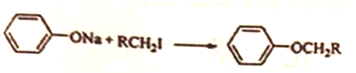

 .
.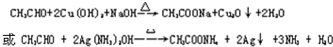 .
.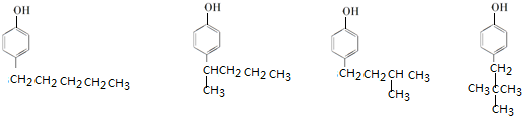 、
、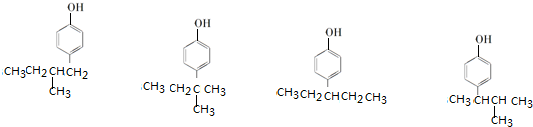 (其中任意两种).
(其中任意两种).