题目内容
对于化学反应方向的确定,下列说法正确的是( )
| A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
| B.温度、压强一定时,吸热的熵增反应一定能够自发进行 |
| C.反应焓变是决定反应能否自发进行的唯一因素 |
| D.固体的溶解过程与熵变无关 |
A
解析试题分析:A.在温度、压强一定的条件下,若体系的自由能ΔG=ΔH-T·ΔS<0,则反应能自发进行;若ΔG=ΔH-T·ΔS>0则反应一定不能自发进行;若ΔG=ΔH-T·ΔS=0,则反应处于平衡状态。因此焓因素和熵因素共同决定一个化学反应的方向。正确。B.温度、压强一定时,放热的熵增反应一定能够自发进行。吸热的熵增反应不一定能够自发进行。错误。C.决定反应能否自发进行的判据除了焓判据外还有熵判据,因此熵变不是的唯一因素。错误。D.固体的溶解过程是体系的混乱程度增大的过程。因此与熵变有关。错误。
考点:考查化学反应方向的确定的影响因素的知识。

练习册系列答案
相关题目
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)  SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是( )
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
在恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:
2A(g)+B(g)  2C(g) ΔH>0。
2C(g) ΔH>0。
达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是( )
| 选项 | x | y |
| A | 再通入A | B的转化率 |
| B | 加入催化剂 | A的体积分数 |
| C | 压强 | 混合气体的总物质的量 |
| D | 温度 | 混合气体的总物质的量 |
下列反应在任意温度下一定能自发进行的是( )
A.2NaCl+2H2O 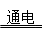 2NaOH+Cl2↑+H2↑ 2NaOH+Cl2↑+H2↑ |
| B.NH3(g)+HCl(g)=NH4Cl(s) ΔH<0 |
| C.CaCO3(s)=CaO(s)+CO2(g) ΔH>0 |
| D.X2Y2(g)=X2(g)+Y2(g) ΔH<0 |
下列各项不正确的是
| A.等物质的量浓度的下列溶液中① NH4Al(SO4)2② NH4Cl,③CH3COONH4,④ NH3·H2O; c(NH4+),由大到小的顺序是①>②>③>④ |
B.室温下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性 |
| C.25℃时,0.1mol/LCH3COOH溶液V1 mL和0.1mol/L NaOH溶液V2mL混合,若V1>V2,则混合溶液的pH一定小于7 |
D.对于反应 ,在任何温度下都能自发进行 ,在任何温度下都能自发进行 |
在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)  2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
| A.图中a点的值为0.15 |
| B.该反应的平衡常数K=0.03 |
| C.温度升高,平衡常数K值减小 |
| D.平衡时A2的转化率为62.5% |
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g) 2z(g) ΔH2>0
2z(g) ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
 A. B. C. D.
A. B. C. D. 2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
2C(g),平衡后增大压强,A的百分含量减小,则n≥2。