题目内容
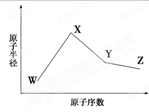
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是

| A.对应简单离子半径X<W |
| B.对应气态氢化物的稳定性Y<Z |
| C.化合物XZW既含离子键也含共价键 |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
D
试题分析:A. W的质子数为18-10=8,所以W为O元素;由于在同一周期的元素,原子序数越大,原子半径就越小。而不同周期的元素,原子核外的电子层数越多,原子半径越大。X原子序数与Ne相差1,结合原子半径可知X为Na元素;Y的单质是一种常见的半导体材料;则Y为Si元素;Z原子序数大于Si,而且其非金属性在同周期元素中最强,那么Z为Cl元素。A. Na+、O2-电子层结构相同。对于电子层结构相同的离子来说,核电荷数越大,离子半径就越小。所以 对应简单离子半径Na+< O2-。正确。B.元素的非金属性越强,对应气态氢化物就越稳定。非金属性Si<Cl,所以稳定性SiH4 <HCl。正确。C.化合物NaClO是离子化合物,既含离子键也含共价键。正确。D. SiO2是酸性氧化物,只能与强碱NaOH发生反应:SiO2+2NaOH=Na2SiO3+H2O,而不能与HClO4发生反应。错误。

练习册系列答案
相关题目
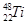 和
和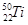 的说法中正确的是( )
的说法中正确的是( )