题目内容
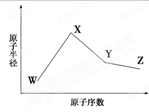
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如下图所示,下列说法一定正确的是


| A.最高价氧化物对应水化物的酸性最强的是W |
| B.Y与Z只能形成一种化合物 |
| C.简单阴离子还原性:Y>W |
| D.Z与Q形成的化合物水溶液可能显酸性 |
D
试题分析:短周期元素W的单质为淡黄色固体,则W是S元素,Y是O元素,X是C元素,因为X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素,则Q是Cl元素,其中Z的原子序数大于8又小于16的金属元素 ,可能是Na、Mg、Al中的一种。A. 在这五种元素中非金属性最强的是Cl,所以最高价氧化物对应水化物的酸性最强的是HClO4。错误。B.若Z是Na元素,则可以形成Na2O、Na2O2两种氧化物。若Z是Mg、Al,则只能形成一种氧化物MgO或Al2O3.错误。C.O、S是同主族的元素。从上到下,元素的非金属性逐渐减弱,则其简单阴离子还原性逐渐增强。元素的非金属性O>S,所以还原性S2->O2-。错误。D. 若Z为Mg或Al,则MgCl2、AlCl3都是强酸弱碱盐,金属阳离子发生水解反应消耗水电离产生的OH-而使溶液中的H+浓度增大,溶液显酸性。正确。

练习册系列答案
相关题目



 A+N2↑+3CO2↑(已配平)。
A+N2↑+3CO2↑(已配平)。