题目内容
【题目】煤气化是有效利用化石能源手段之一,有关反应如下:
①C + H2O![]() CO + H2 ② CO + H2O
CO + H2 ② CO + H2O![]() CO2 + H2
CO2 + H2
获得的气体称为水煤气。某研究性学习小组为探究气体的成分进行了如下实验:
【实验】 使水蒸气通过灼热的焦炭,收集反应后流出的气体。
【提出假设】 对气体的成份提出了三种假设。
假设1:该气体是 CO、H2 、H2O。
假设2:该气体是 CO2、H2 、H2O 。
(1)假设 3: 。
【设计实验方案,验证假设】
他们拟用下图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)。

(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):混合气→ dc→ → →ij → → → →ij ;
(3)仪器A中需加入试剂的是 ,其中反应的化学方程式是 ;
(4)仪器B中需加入试剂的名称是 ,其作用是 ;
【思考与交流】
(5)本实验的尾气需要处理,处理的方法为 。
【答案】
(1)CO、H2、H2O、CO2;
(2)ij;gh;ef;ab;dc;
(3)氧化铜(CuO);CuO+H2![]() Cu+H2O,CuO+CO
Cu+H2O,CuO+CO![]() Cu+CO2;
Cu+CO2;
(4)无水硫酸铜;检验H2O(g);
(5)可在装置最后的导管口处放一点燃的酒精灯,将气体燃烧后排放(或用气球收集)。
【解析】
试题分析:
(1)根据反应原理,混合气体组成存在三种情况,第三种情况还可能为:CO、H2、H2O、CO2,故答案为:CO、H2、H2O、CO2;
(2)为了验证混合气中含CO、H2、H2O、CO2,实验仪器的连接先后顺序为:检验水分→检验二氧化碳→除掉二氧化碳→除掉水分→还原装置→检验水分→检验二氧化碳,仪器连接顺序为:混合气体→dc→ij→gh→ef→ab→dc→ij,故答案为:ij;gh;ef;ab;dc;
(3)仪器A用于检验氢气和一氧化碳,可以选用氧化铜,利用氢气、一氧化碳加热还原氧化铜完成检验,反应的化学方程式为:CuO+H2![]() Cu+H2O,CuO+CO
Cu+H2O,CuO+CO![]() Cu+CO2;故答案为:氧化铜(CuO);CuO+H2
Cu+CO2;故答案为:氧化铜(CuO);CuO+H2![]() Cu+H2O,CuO+CO
Cu+H2O,CuO+CO![]() Cu+CO2;
Cu+CO2;
(4)白色的无水硫酸铜遇水后变为蓝色,所以可在装置干燥管C中加入无水硫酸铜(CuSO4),通过观察颜色是否改变来确定是否有水蒸气的生成,故答案为:无水硫酸铜;检验H2O(g);
(5)一氧化碳有毒,直接排放到空气中会污染环境,可在装置最后的导管口处放一点燃的酒精灯,利用燃烧的方法消除CO的污染,或用气球收集尾气,防止CO污染空气。故答案为:可在装置最后的导管口处放一点燃的酒精灯,将气体燃烧后排放(或用气球收集)。

【题目】硫代硫酸钠晶体(Na2S2O3·5H2O,式量248) 可用于照相行业的定影剂。它易溶于水,且溶解度随温度升高而显著增大,难溶于乙醇,加热时易分解,实验室模拟工业制备硫代硫酸钠晶体通常有两种方法。(硫单质不溶于水,微溶于酒精)
I 亚硫酸钠法:Na2SO3+S+5H2O=Na2S2O3·5H2O,简易实验流程如下:

(1)硫粉用乙醇润湿的目的是 ;
(2)洗涤粗产品,下列洗涤剂最合适的是 ;
A.冰水 B.热水 C.乙醇 D.乙醇-水混合溶液
(3)所得粗产品一般通过 方法提纯;
II硫化碱法:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,主要实验装置如下:
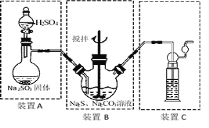
(4)装置C中可放入 ;
A.BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.NaOH溶液
(5)为测定粗产品中Na2S2O35H2O的纯度。某兴趣小组称取5.0 g粗产品配成250mL溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.01mol/L KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+=3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当蓝色褪去且半分钟不变色时到达滴定终点。实验数据如下表:
滴定次数 | 1 | 2 | 3 |
消耗Na2S2O3溶液(mL) | 19.98 | 21.18 | 20.02 |
该产品的纯度是 ;
(6)硫代硫酸钠产率受温度、pH影响如下图:

下列说法不正确的是 。
A.生成Na2S2O3一定是放热反应
B. 制备应采取较低温度
C.Na2S2O3一定能和0.1mol·L-1的硫酸发生反应
D.控制pH和温度,可以提高Na2S2O3的产率







