题目内容
7.感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广泛的新型高分子材料.其结构简式为: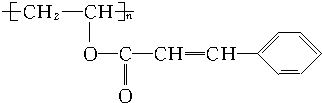
已知它是由两种单体聚合而成的,写出聚合反应的方程式
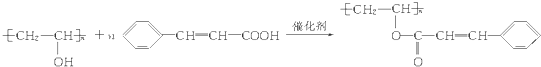 .
.
分析 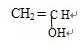 和
和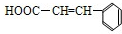 反应生成酯
反应生成酯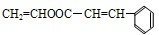 ,由
,由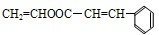 发生加成聚合反应生成该新型高分子化合物.
发生加成聚合反应生成该新型高分子化合物.
解答 由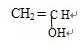 和
和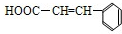 反应生成该高分子化合物要经过酯化反应、加聚反应两步,①酯化反应:
反应生成该高分子化合物要经过酯化反应、加聚反应两步,①酯化反应: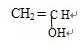 +
+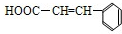 →
→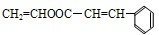 +H2O;②加聚反应:n
+H2O;②加聚反应:n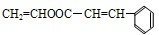 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$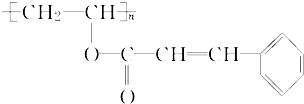 ,
,
故答案为: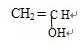 +
+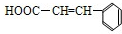 →
→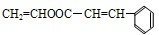 +H2O.
+H2O.
点评 本题考查了有机高分子化合物的结构和性质,侧重于酯化反应、加聚反应和官能团的考查,把握好有机反应中官能团的变化是解答此类题的关键.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
18.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
(1)砷原子核外电子排布式为1s22s22p63s23p63d104s24p3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(3)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3.
(1)砷原子核外电子排布式为1s22s22p63s23p63d104s24p3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(3)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4;但氨气分子间还存在氢键,则NH3的沸点高于PH3
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是C-H键的键能大于Si-H键的键能,N-H键的键能大于P-H键的键能,因此分解温度CH4的分解温度高于SiH4,NH3的分解温度高于PH3.
15.已知CH3CH2Br+2Na+CH3CH2Br→CH3CH2CH2CH3+2NaBr.下列有机物发生这种反应可生成X,若X与环丙烷互为同系物,则能生成X的是( )
| A. | CH3CH2CH2Cl | B. | CH3CHBrCH(CH3)CH2Br | ||
| C. | CH3CHBrCH2CH2Br | D. | CH3CH2Br |
2.高分子分离膜可以让某些物质有选择地通过而将物质分离,下列应用不属于高分子分离膜应用范围的是( )
| A. | 分离工业废水,回收废液中的有用成分 | |
| B. | 将化学能转换成电能,将热能转换成电能 | |
| C. | 食品工业中,浓缩天然果汁、乳制品加工和酿酒 | |
| D. | 海水淡化 |
12.下列说法正确的是( )
| A. | 甲醛是甲基跟醛基相连而构成的 | |
| B. | 饱和一元醛的通式可简写为RCOH | |
| C. | 在银镜反应中乙醛体现了氧化性 | |
| D. | 饱和一元脂肪醛的分子组成符合通式CnH2nO |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1的Ca(ClO)2溶液中含ClO-数目为2NA | |
| B. | 含1molH2SO4的浓硫酸和足量的锌完全反应,转移的电子数为2NA | |
| C. | 1mol Mg在空气中完全燃烧生成MgO和Mg3N2,失去2NA个电子 | |
| D. | 某密闭容器盛有0.1molN2,0.3molH2,在一定条件下反应,转移的电子数为0.6NA |
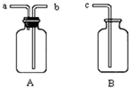 如图所示用一起A、B和胶管组成装置收集NO气体(仪器A已经气密性检查;除水外不能选用其他试剂)正确的操作步骤是:在A中加满水,盖紧瓶塞,用胶管连接b和c接口,由a导入NO气体,水通过b和c排入B中.
如图所示用一起A、B和胶管组成装置收集NO气体(仪器A已经气密性检查;除水外不能选用其他试剂)正确的操作步骤是:在A中加满水,盖紧瓶塞,用胶管连接b和c接口,由a导入NO气体,水通过b和c排入B中.
 (1)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为27.6%.若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为48.3%.
(1)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为27.6%.若其中CO和N2的物质的量之比为1:1,则混合气体中氧元素的质量分数为48.3%.