题目内容
下列叙述正确的是( )
| A、同种元素的原子均具有相同的质子数和中子数 |
| B、不同元素的原子构成的分子只含极性键 |
| C、第三周期中的非金属元素的气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱 |
| D、第ⅦA族元素从上到下单质及对应的气态氢化物的沸点均逐渐升高 |
考点:原子构成,元素周期表的结构及其应用,元素周期律的作用,极性键和非极性键
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:A、同种元素的原子质子数相同,中子数可能不同;
B、不同元素的原子构成的分子可能也含非极性键;
C、非金属元素非金属性越弱,气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱;
D、卤族元素从上到下单质的沸点均逐渐升高,但气态氢化物中HF中含氢键,沸点最高.
B、不同元素的原子构成的分子可能也含非极性键;
C、非金属元素非金属性越弱,气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱;
D、卤族元素从上到下单质的沸点均逐渐升高,但气态氢化物中HF中含氢键,沸点最高.
解答:
解:A、同种元素的原子质子数相同,中子数可能不同,如同位素,故A错误;
B、不同元素的原子构成的分子可能也含非极性键,如双氧水,故B错误;
C、第三周期中的非金属元素的气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱,故C正确;
D、卤族元素从上到下单质的沸点均逐渐升高,但气态氢化物中HF中含氢键,沸点最高,而HCl、HBr、HI的相对分子质量在增大,气态氢化物的沸点升高,故D错误;
故选C.
B、不同元素的原子构成的分子可能也含非极性键,如双氧水,故B错误;
C、第三周期中的非金属元素的气态氢化物还原越强,对应元素的最高价含氧酸酸性越弱,故C正确;
D、卤族元素从上到下单质的沸点均逐渐升高,但气态氢化物中HF中含氢键,沸点最高,而HCl、HBr、HI的相对分子质量在增大,气态氢化物的沸点升高,故D错误;
故选C.
点评:本题主要考查了原子的种类、化学键、元素周期律等知识,难度不大,注意知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、稀有气体原子序数越大,熔点越低 |
| B、同周期元素的原子半径越小,气态氢化物还原性越弱 |
| C、晶体中分子间作用力越强,分子越稳定 |
| D、卤族元素的氢化物,相对分子质量越大,熔沸点越高 |
下列熔合物的固体属于合金的是( )
①Al与Cu ②Fe与C ③K与Na ④Al与Si.
①Al与Cu ②Fe与C ③K与Na ④Al与Si.
| A、①②③④ | B、①③ |
| C、②④ | D、①④ |
下列变化过程放热的是( )
| A、H2O(l)→H2O(g) |
| B、2HI(g)→H2(g)+I2(g)+Q Q=-14.9 kJ/mol |
| C、形成化学键时共放出能量862 kJ的化学反应 |
D、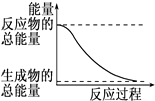 能量变化如图所示的化学反应 |
下列说法正确的是( )
| A、干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,Na2O2在这个反应中只做氧化剂 |
| B、C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(l);△H=-1367.0kJ/mol(燃烧热) |
| C、过量的NaHCO3溶液与Ca(OH)2溶液反应的离子方程式是:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
下列离子方程式正确的是( )
| A、将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH-→CaCO3↓+H2O |
| B、Fe(OH)3溶于氢碘酸:2Fe(OH)3+6H++2I-→2Fe2++I2+6H2O |
| C、向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42-离子沉淀完全Al3++2SO42-+2Ba2++4OH-→AlO2-+2BaSO4↓+2H2O |
| D、4mol?L-1的NaAlO2溶液和7mol?L-1的HCl等体积互相均匀混合4AlO2-+7H++H2O→3Al(OH)3↓+Al3+ |