题目内容
某金属氯化物MCl2 27g,含有0.40molCl-,则该氯化物的物质的量为______,摩尔质量为 ,金属M的相对原子质量为 。
0.2 mol ,135 g/mol ,64
解析试题分析:由该金属氯化物的电离方程式:MCl2 =M2++2Cl-可得该氯化物的物质的量为0.2mol.n=m/M.所以摩尔质量为:M=m/n=27g/0.2mol=135g/mol.其相对分子质量为135=M+2×35.5 所以M=64.
考点:考查物质的量与摩尔质量、相对分子质量的关系及计算等的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”溶液中含有的成分,阅读后回答下列问题:
| 成分 | 质量(g) | 摩尔质量(g ·mol—1) |
| 蔗糖 | 25.0 | 342 |
| 硫酸钾 | 0.3 | 174 |
| 阿司匹林 | 0.2 | 180 |
| 高锰酸钾 | 0.3 | 158 |
| 硝酸银 | 0.1 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)500mL“鲜花保鲜剂”中含有AgNO3的物质的量为_______mol(只列式,不计算结果);“鲜花保鲜剂”中K+(阿司匹林和蔗糖中不含K+)的物质的量浓度为___________mol/L。
(注意:第(2)题空格只要求写表达式,不需要化简与计算)
(3)由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是_________(填操作序号)
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②定容时俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水

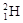 和
和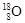 组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。
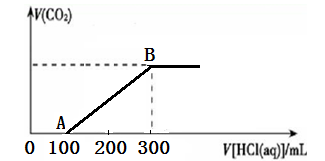
组成的水分子的物质的量 mol,其中含中子数为 mol,电子数为 个。 MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。
MnCl2+2H2O+Cl2↑。若0.1 molMnO4与足量的浓盐酸充分反应,则有 mol HCl被氧化,转移电子的物质的量为 mol,产生的Cl 2在标准状况下的体积为 L。