题目内容
共价键、离子键和范德华力都是微观粒子之间的不同作用力,下列物质:①Na2O2;②SiO2;③碘;④金刚石;⑤NaCl;⑥白磷,其中含有两种作用力的组合是( )
| A、①②⑤ | B、①③⑥ |
| C、②④⑥ | D、①②③⑥ |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,离子晶体中含有离子键,以共价键结合的物质可能为原子晶体,也可能为分子晶体,在分子晶体中还存在分子间作用力,以此来解答.
解答:
解:①Na+和O22-之间形成离子键、O22-中氧原子之间形成共价键,故①正确;
②SiO2为原子晶体,只含共价键,故②错误;
③碘分子内存在共价键,分子间存在分子间作用力,故③正确;
④金刚石是原子晶体,只存在共价键,故④错误;
⑤NaCl为离子晶体,只含有离子键,故⑤错误;
⑥白磷分子内磷原子之间形成共价键,而分子与分子间为范德华力,故⑥正确.
故选B.
②SiO2为原子晶体,只含共价键,故②错误;
③碘分子内存在共价键,分子间存在分子间作用力,故③正确;
④金刚石是原子晶体,只存在共价键,故④错误;
⑤NaCl为离子晶体,只含有离子键,故⑤错误;
⑥白磷分子内磷原子之间形成共价键,而分子与分子间为范德华力,故⑥正确.
故选B.
点评:本题考查化学键和晶体,注意化学键的形成规律及分子晶体中存在分子间作用力即可解答,注意石墨中的分子间作用力是学生解答的难点,难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
下列金属中,可用于制造常温下盛放浓硫酸的容器的是( )
| A、Mg | B、Cu | C、Al | D、Zn |
下列表示溶液中所发生反应的离子方程式正确的是( )
| A、AlCl3溶液与过量氨水混合:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
| B、偏铝酸钠溶液中通入过量二氧化碳:2AlO2-+CO2+2H2O═2Al(OH)3↓+CO32- | ||||
C、用铜电极做盐酸的导电实验:2H++2Cl-
| ||||
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
实验室用于检验盐酸和其他电离时能产生Cl-的化合物的试剂是( )
| A、稀盐酸和石灰水 |
| B、氢氧化铁 |
| C、氯化钡溶液和稀硝酸 |
| D、硝酸银溶液和稀硝酸 |
有Xn+、Ym+、Zn-三种主族元素的离子,已知它们各自带有的电荷的数值m>n(m,n均为正整数),且X、Y、Z三种原子的M电子层中的电子数均为奇数.若X、Y、Z原子序数依次增加,下列说法中不正确的是( )
| A、它们的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强 |
| B、三种离子Xn+、Ym+、Zn-具有相同的电子层结构 |
| C、它们都在第三周期 |
| D、X单质有还原性,Z单质具有氧化性 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,64g S02含有的原子总数为3NA |
| C、标准状况下,11.2L SO3中含有分子的数目为0.5NA |
| D、常温常压下,1mol Na2O2中阴离子数为2NA |
aXn-和bYm+是由短周期元素形成的最简单离子,已知Xn-比Ym+多两个电子层,下列说法中正确的是( )
| A、X只能是第三周期元素 |
| B、Y不可能是第二周期元素 |
| C、Y一定是氢元素 |
| D、a-b+n+m等于10或16 |
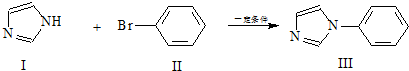
 ,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为:
,Ⅴ与氢氧化钠醇溶液加热条件下反应的方程式为: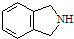 与
与 也可以发生类似反应①的反应,参加反应的分子数为2:1,则生成的产物的结构简式为
也可以发生类似反应①的反应,参加反应的分子数为2:1,则生成的产物的结构简式为