题目内容
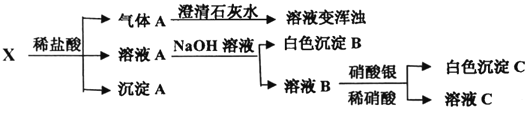
【题目】Ⅰ.某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.800g 试样溶于水,加入过量KI 固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3 标准溶液滴定,到达滴定终点时,平均消耗Na2S2O3 标准溶液40.00 mL。(已知:2Cu2++4I-=2CuI↓+I2;I2+2S2O32-=S4O62-+2I-。)
(1)可选用________作滴定指示剂,滴定终点的现象是________________。
(2)该试样中CuCl2·2H2O 的质量百分数为________________。
Ⅱ.25℃,两种酸的电离平衡常数如表,按要求回答下列问题。
K1 | K2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
(1)用离子方程式表示亚硫酸钠溶液呈碱性的原因________________________________。
(2)浓度均为0.1mol/L的Na2SO3和Na2CO3的溶液中SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为________________________________。
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式________________________________。
【答案】淀粉溶液 淀粉由蓝色变成无色且半分钟不变化 85.5% SO32-+H2O![]() HSO3-+OH- SO32->CO32->HCO3->HSO3- Na2SO3+CO2+H2O= NaHSO3+ NaHCO3
HSO3-+OH- SO32->CO32->HCO3->HSO3- Na2SO3+CO2+H2O= NaHSO3+ NaHCO3
【解析】
Ⅰ.(1)向含碘的溶液中加入淀粉溶液,溶液变蓝色,再向溶液中加入Na2S2O3溶液,由于碘被Na2S2O3还原为碘离子,溶液蓝色逐渐褪去,当溶液蓝色刚好消失时,碘正好完全反应,从而进行滴定终点的判定;
(2)根据电子转移守恒及I2+2S2O32-═S4O62-+2I-,可得关系式:2Cu2+~I2~2Na2S2O3,则n(CuCl22H2O)=n(Na2S2O3),根据m=nM计算CuCl22H2O的质量,进而计算CuCl22H2O的质量百分数;
Ⅱ.(1)SO32-发生水解,离子方程式为:SO32-+H2O![]() HSO3-+OH-,使溶液呈碱性;
HSO3-+OH-,使溶液呈碱性;
(2)SO32-水解程度小于CO32-,浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-);
(3)亚硫酸钠溶液中通入少量CO2气体的化学方程式为:Na2SO3+CO2+H2O= NaHSO3+ NaHCO3。
Ⅰ.(1)硫代硫酸钠滴定碘单质,利用碘单质遇淀粉变蓝选择指示剂为淀粉,滴入最后一滴Na2S2O3溶液,溶液蓝色褪去,且半分钟内不变色,说明滴定到达终点,
故答案为:淀粉溶液;淀粉由蓝色变成无色且半分钟不变化。
(2)由2Na2S2O3+I2═Na2S4O6+2NaI,2Cu2++4I-═2CuI↓+I2,可得关系式:2Cu2+~I2~2Na2S2O3,则n(CuCl22H2O)=n(Na2S2O3)=0.1000mol/L×0.0400L=0.004mol,故m(CuCl22H2O)=0.004mol×171g/mol=0.684g,所以试样中CuCl22H2O的质量百分数为0.684g/0.800g×100%=85.8%,
故答案为:85.5%。
Ⅱ.(1)Na2SO3是强电解质,全部电离,电离方程式为:Na2SO3=2Na++SO32-,SO32-发生水解,离子方程式为:SO32-+H2O![]() HSO3-+OH-,使溶液呈碱性,
HSO3-+OH-,使溶液呈碱性,
故答案为:SO32-+H2O![]() HSO3-+OH-。
HSO3-+OH-。
(2)依据电离平衡常数大小比较,H2SO3Ki1=1.54×10-2、Ki2=1.02×10-7,H2CO3Ki1=4.3×10-7、Ki2=5.6×10-11。说明SO32-水解程度小于CO32-,浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-),
故答案为:c(SO32-)>c(CO32-)>c(HCO3-)>c(HSO3-)。
(3)由于H2SO3Ki1=1.54×10-2、Ki2=1.02×10-7,H2CO3Ki1=4.3×10-7、Ki2=5.6×10-11,所以亚硫酸钠溶液中通入少量CO2气体的化学方程式为:Na2SO3+CO2+H2O=NaHSO3+NaHCO3,
故答案为:Na2SO3+CO2+H2O=NaHSO3+NaHCO3。

【题目】氮是地球上含量最丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(图中涉及物质为气态)
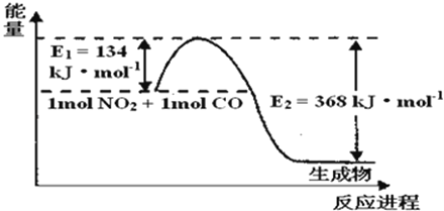
(1)如图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式______。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表,
2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表,
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请完成下列问题:
①试比较K1、K2的大小,K1______K2(填写“>”、“=”或“<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_______(填序号字母)。
a .容器内N2,H2,NH3的浓度之比为1:3:2 b. υ(N2)正=3υ(H2)逆
c .容器内压强保持不变 d. 混合气体的密度保持不变
③在400℃时,当测得NH3和N2,H2的物质的量分别为1mol和2mol,3mol时,则该反应的υ(N2)正______υ(N2)逆(填写“>,“=”或“<”)。