题目内容
6.下列离子方程式书写正确的是( )| A. | 少量稀HNO3中加入足量铁粉:Fe+4H++NO3-═NO↑+Fe3++2H2O | |
| B. | 以石墨作电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | NH4HCO3溶液中加入过量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
分析 A.反应生成硝酸亚铁、NO和水;
B.电解生成氢氧化镁、氢气、氯气;
C.漏写铵根离子与碱的反应;
D.遵循电子、电荷守恒.
解答 解:A.少量稀HNO3中加入足量铁粉的离子反应为3Fe+8H++2NO3-═2NO↑+3Fe2++4H2O,故A错误;
B.以石墨作电极电解MgCl2溶液的离子反应为Mg2++2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,故B错误;
C.NH4HCO3溶液中加入过量石灰水的离子反应为NH4++HCO3-+Ca2++2OH-═CaCO3↓+H2O+NH3.H2O,故C错误;
D.Na2SO3溶液使酸性KMnO4溶液褪色的离子反应为5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O,遵循电子、电荷守恒,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
16.下列说法中不正确的是( )
| A. | 维勒用无机物合成了尿素,突破了无机物与有机物的界限 | |
| B. | 分子式为C4H8的有机物可能存在4个C-C单键 | |
| C. | (CH3)3CCH2CH(C2H5)CH3 可命名为2,2-二甲基-4-乙基戊烷,核磁共振氢谱有6组峰 | |
| D. | 尼龙、棉花、天然橡胶、ABS树脂都是由高分子化合物组成的物质 |
11.如图所示的装置,C.D.E.F.X.Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是( )


| A. | 电源B极是正极 | |
| B. | 欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 | |
| C. | 甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2 | |
| D. | 装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |
15.下列物质的应用不正确的是( )
| A. | SO2可用于漂白纸浆 | B. | 碱石灰可用于干燥氯气 | ||
| C. | 氢氟酸可用于蚀刻玻璃 | D. | 碳酸氢钠可用于中和胃酸 |
16.叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
| A. | HN3水溶液中微粒浓度大小顺序为:c(H+)>c( N3-)>c(HN3)>c(OH-) | |
| B. | NaN3水溶液中离子浓度大小顺序为:c(Na+)>c( N3-)>c(OH-)>c(H+) | |
| C. | HN3与NH3作用生成的叠氮酸铵是强电解质 | |
| D. | N3-与CO2互为等电子体 |
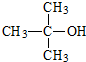

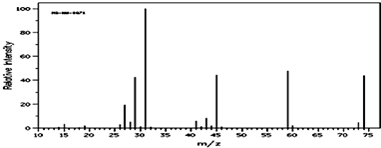


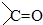 的加成类似于
的加成类似于 的加成)
的加成) .
.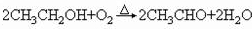 .
. .
.