题目内容
14.酸牛奶是人们喜爱的一种营养饮料.酸牛奶中有乳酸菌可产生乳酸等有机酸,使酸碱度降低,有效地抑制肠道内病菌的繁殖.酸牛奶中的乳酸可增进食欲,促进胃液分泌,增强肠胃的消化功能,对人体具有长寿和保健作用,乳酸的结构为:
工业上它可由乙烯来合成,方法如下:
CH2=CH2$→_{催化剂}^{HCl}$A$→_{△}^{NaOH/H_{2}O}$B$→_{△}^{O_{2}(Cu)}$CH3CHO$→_{加成}^{HCN}$C

(提示:(1)CH3Cl+NaOH$\stackrel{△}{→}$CH3OH+NaCl,(2)
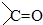 的加成类似于
的加成类似于 的加成)
的加成)(1)乳酸所含的官能团的名称是羧酸、羟基.
(2)写出下列转化的化学方程式:
①A的生成
 .
.②C的生成
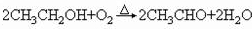 .
.③乳酸在一定条件合成聚乳酸nCH3CH(OH)COOH$\stackrel{一定条件}{→}$nH2O+
 .
.(3)写出符合下列要求的乳酸的所有同分异构体的结构简式HCOOCH2CH2OH、HCOOCH(OH)CH3
a、属于酯类,b、含有-OH,c、能发生银镜反应.
分析 由合成路线可知,乙烯发生加成反应生成A,A为CH3CH2Cl,A碱性水解生成B,B为CH3CH2OH,B氧化生成乙醛,乙醛与HCN加成生成C,则C为CH3CHOHCN,最后水解生成乳酸,然后结合有机物的结构与性质来解答.
解答 解:由合成路线可知,乙烯发生加成反应生成A,A为CH3CH2Cl,A碱性水解生成B,B为CH3CH2OH,B氧化生成乙醛,乙醛与HCN加成生成C,则C为CH3CHOHCN,最后水解生成乳酸,
(1)乳酸含-COOH、-OH,名称分别为羧酸、羟基,
故答案为:羧酸、羟基;
(2)①A的生成反应为 ,
,
②C的生成反应为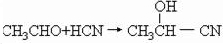 ,
,
③乳酸在一定条件合成聚乳酸的反应为n CH3CH(OH)COOH $\stackrel{一定条件}{→}$nH2O+ ,
,
故答案为:① ;②
;②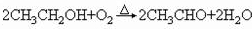 ;③n CH3CH(OH)COOH $\stackrel{一定条件}{→}$nH2O+
;③n CH3CH(OH)COOH $\stackrel{一定条件}{→}$nH2O+ ;
;
(3)根据条件a、属于酯类,b、含有-OH,c、能发生银镜反应,说明有醛基,则符合条件的乳酸的所有同分异构体的结构简式为HCOOCH2CH2OH、HCOOCH(OH)CH3,
故答案为:HCOOCH2CH2OH、HCOOCH(OH)CH3.
点评 本题考查有机物的合成,为高频考点,把握烯烃、醇、醛的性质及合成流程为解答的关键,注意官能团与性质的关系、结构与性质的关系及习题中信息,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.某元素的一个原子形成的离子可表示为baXn-,下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A. | baXn-中含有的中子数为a+b | B. | baXn-中含有的电子数为a-n | ||
| C. | X原子的质量约为(b/NA)g | D. | 此元素的相对原子质量为b |
9.下列说法不正确的是( )
| A. | 探究温度对反应速率影响时,应先分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度后再混合,不是先将两种溶液混合后再用水浴加热 | |
| B. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| C. | 使用含有氯化钠的融雪剂会加快铁桥梁的腐蚀 | |
| D. | 判断皂化反应是否完全,可取反应后的混合液滴入热水中 |
19.工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
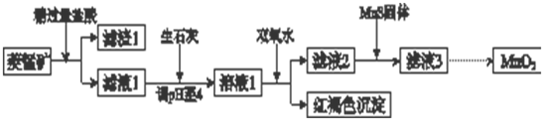
已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol/L
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是增大接触面积,提高反应速率.盐酸溶解MnCO3的化学方程式是MnCO3+2HCl=MnCl2+CO2↑+H2O.
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+.
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS.
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:
□Mn2++□ClO3-+□4H2O=□Cl2↑;+□5MnO2+□8H+.
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+.
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2.检验Cl2的操作是将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成.
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是其它条件不变下,增大Mn2+浓度[或增大c(Mn2+)/c(Cl-)],有利于Mn2+放电(不利于Cl-放电).

已知:
生成氢氧化物沉淀的pH
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是增大接触面积,提高反应速率.盐酸溶解MnCO3的化学方程式是MnCO3+2HCl=MnCl2+CO2↑+H2O.
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+.
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS.
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:
□Mn2++□ClO3-+□4H2O=□Cl2↑;+□5MnO2+□8H+.
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+.
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2.检验Cl2的操作是将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成.
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是其它条件不变下,增大Mn2+浓度[或增大c(Mn2+)/c(Cl-)],有利于Mn2+放电(不利于Cl-放电).
6.下列离子方程式书写正确的是( )
| A. | 少量稀HNO3中加入足量铁粉:Fe+4H++NO3-═NO↑+Fe3++2H2O | |
| B. | 以石墨作电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | NH4HCO3溶液中加入过量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
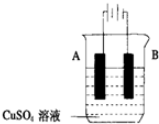
3.如图,烧杯中的溶质均足量,a、b、c、d、e均为石墨电极,通电一段时间后,a电极上有红色物质析出,以下说法正确的是( )
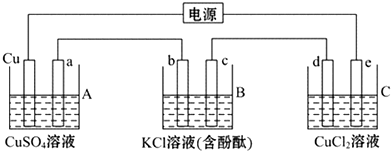

| A. | e电极上可以析出使湿润的淀粉KI试纸变蓝的气体 | |
| B. | c电极周围溶液变红 | |
| C. | A烧杯内溶液的pH升高 | |
| D. | B烧杯中加一定量的KCl固体可恢复原状 |