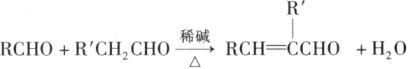
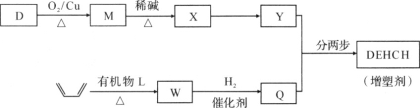
题目内容
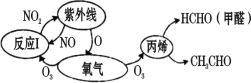
【题目】大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是( )
A. NO2不是酸性氧化物B. O2和O3是氧的两种同素异形体
C. 反应I属于氧化还原反应D. 烟雾是一种固溶胶,其分散剂是空气
【答案】D
【解析】
由示意图可知,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物光化学烟雾的反应过程为二氧化氮在紫外线作用下分解生成一氧化氮和氧原子,氧原子与氧气反应生成臭氧,臭氧与一氧化氮反应生成二氧化氮,与丙烯反应生成甲醛和乙醛。
A项、酸性氧化物与水反应只生成化合价相同的酸,NO2与水反应生成硝酸和NO,不是酸性氧化物,故A正确;
B项、由同种元素组成的不同单质互称为同素异形体,O2和O3是氧元素的两种单质,互称为同素异形体,故B正确;
C项、反应I为臭氧与一氧化氮反应生成二氧化氮,反应中存在元素化合价的变化,属于氧化还原反应,故C正确;
D项、烟雾是一种气溶胶,其分散剂是空气,故D错误。
故选D。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】甲醇是重要的化工原料,利用煤化工中生产的CO、CO2和H2可制取甲醇等有机物,发生的反应有:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-99kJ·mol-1
CH3OH(g) △H1=-99kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
相关物质的化学键键能数据如下:
化学键 | C=O(CO2) | H—H | C—O | H—O | C—H |
E/(kJ·mol-1) | 803 | 436 | 343 | 465 | 413 |
(1)该反应△H2=___________。
(2)关于反应①下列说法,正确的是___________。
A.该反应在任何温度下都能自发进行
B.升高温度,正反应速率增大,逆反应速率减小
C.使用催化剂,不能提高CO的转化率
D.增大压强,该反应的化学平衡常数不变
(3)在某温度下,将1.0moCO与2.0molH2充入2L的空钢瓶中,发生反应①,在第5min时达到化学平衡状态,此时甲醇的物质的量分数为0.1。在第10min、20min时分别改变反应条件,甲醇的浓度在不同条件下的变化状况如下图所示:
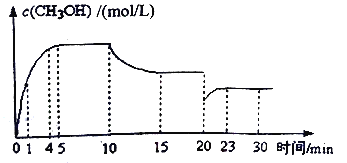
①从反应开始到5min时,生成甲醇的平均速率为___________。
②H2的平衡转化率α=___________%,化学平衡常数K=___________。
③1min时,υ正___________υ逆(填“大于”“小于”或“等于”)
④1mim时υ正___________4min时υ逆(填“大于”“小于”或“等于”)
⑤比较甲醇在7~8min、12~13min和25~27min时平均反应速率[平均反应速率分别以υ(7~8)、υ(12~13)、υ(25~27)表示的大小_________________________________。
③若将钢瓶换成同容积的绝热容器,重复上述试验,平衡时甲醇的物质的量分数___________0.1。(填“>”、“<”或“=”)