��Ŀ����
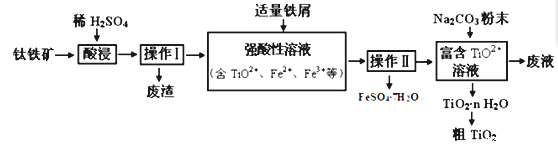
����Ŀ���ѺϽ��Ǻ��캽�չ�ҵ����Ҫ���ϡ�����������Ҫ�ɷ���TiO2��Fe��������Ʊ�TiO2�Ȳ�Ʒ��һ�ֹ�������ʾ��ͼ������ʾ��
��֪����TiO2+��ˮ�⣬ֻ�ܴ�����ǿ������Һ��
��TiCl4���۵�-25.0�棬�е�136.4�棻SiCl4���۵�-68.8�棬�е�57.6��
�ش��������⣺
��1��д�����������ʱ����Ҫ�ɷ�TiO2��Ӧ�����ӷ���ʽ_______��������м��������______��
��2������������ľ������������______________________��
��3������TiO2+��Һ���м���Na2CO3��ĩ�õ�����TiO2��nH2O������ǡ����ԭ���ͻ�ѧ���������ԭ��___________����Һ�����ʵ���Ҫ�ɷ���____________���ѧʽ����
��4���ý��ʯ����Ҫ��TiO2��Ϊԭ�ϣ����ú��أ�Hunter���������ѵ���������ͼ��ʾ��

д�������Ȼ�¯�з�����Ӧ�Ļ�ѧ����ʽ_______________���Ƶõ�TiCl4Һ���г���������SiCl4���ʣ��ɲ���_______________������ȥ����ʹ16gTiO2��ȫת��ΪTi��������ҪNa���ʵ���Ϊ___________��
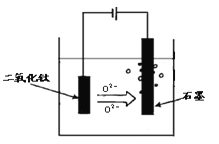
��5��TiO2ֱ�ӵ�ⷨ������������һ�ֽ��Ƚ��ķ��������ҺΪij�ֿ��Դ���O2-���ӵ������Σ�ԭ����ͼ��ʾ�����������缫��ӦΪ��______________________���������������缫�ϻ����������ɣ���������ܺ���_______________��
���𰸡� TiO2+2H+=TiO2++H2O ʹFe3+��ԭΪFe2+ ����Ũ������ȴ�ᾧ������(ϴ��) ��Һ�д���ˮ��ƽ��TiO2++(n+1)H2O![]() TiO2nH2O+2H+�������Na2CO3��ĩ��H+��Ӧ����������Һ��c(H+)���ٽ�ˮ��ƽ��������TiO2nH2O�ķ����ƶ� Na2SO4 TiO2+2C+2Cl2
TiO2nH2O+2H+�������Na2CO3��ĩ��H+��Ӧ����������Һ��c(H+)���ٽ�ˮ��ƽ��������TiO2nH2O�ķ����ƶ� Na2SO4 TiO2+2C+2Cl2![]() TiCl4+2CO ����(�����) 0.8mol TiO2+4e-=Ti+2O2- O2��CO��CO2
TiCl4+2CO ����(�����) 0.8mol TiO2+4e-=Ti+2O2- O2��CO��CO2
��������������Ҫ��������Ʊ�TiO2�Ȳ�Ʒ��һ�ֹ������̵����ۡ�
��1�����������ʱ����Ҫ�ɷ�TiO2��Ӧ��ΪTiO2+���÷�Ӧ�����ӷ���ʽΪTiO2+2H+=TiO2++H2O��������м��������ʹFe3+��ԭΪFe2+��
��2�������������ľ����������������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�
��3����������TiO2+��Һ���м���Na2CO3��ĩ�õ�����TiO2��nH2O����ԭ��Ϊ����Һ�д���ˮ��ƽ����TiO2++(n+1)H2O![]() TiO2nH2O+2H+�������Na2CO3��ĩ��H+��Ӧ����������Һ��c(H+)���ٽ�ˮ��ƽ��������TiO2nH2O�ķ����ƶ�����Һ�����ʵ���Ҫ�ɷ������������
TiO2nH2O+2H+�������Na2CO3��ĩ��H+��Ӧ����������Һ��c(H+)���ٽ�ˮ��ƽ��������TiO2nH2O�ķ����ƶ�����Һ�����ʵ���Ҫ�ɷ������������![]() ��Na2CO3������Na+��ɵ�Na2SO4��
��Na2CO3������Na+��ɵ�Na2SO4��
��4�������Ȼ�¯�з�����Ӧ�Ļ�ѧ����ʽΪTiO2+2C+2Cl2![]() TiCl4+2CO���Ƶõ�TiCl4Һ���г���������SiCl4���ʣ��ɲ���������ȥ����ʹ16g��0.2molTiO2��ȫת��ΪTi��������ҪNa���ʵ���Ϊ0.2mol��4=0.8mol��
TiCl4+2CO���Ƶõ�TiCl4Һ���г���������SiCl4���ʣ��ɲ���������ȥ����ʹ16g��0.2molTiO2��ȫת��ΪTi��������ҪNa���ʵ���Ϊ0.2mol��4=0.8mol��
��5�������缫��ӦΪ��TiO2+4e-=Ti+2O2-���������������缫�ϻ����������ɣ���������ܺ���O2-�������ɵ�O2���Լ�O2�ڵ���¶�����ʯī�缫��Ӧ���ɵ�CO��CO2��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�