题目内容
【题目】在反应2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O中,下列说法正确的是( )
A. 氧化产物与还原产物物质的量之比是2∶5
B. 被氧化的HCl占参加反应HCl总分子数的![]()
C. KMnO4只有一部分发生还原反应
D. KMnO4与HCl恰好分别完全发生还原反应和氧化反应
【答案】B
【解析】试题分析:A、氯化氢是还原剂,氧化产物是氯气。高锰酸钾是氧化剂,还原产物是氯化锰,则根据方程式可知氧化产物与还原产物粒子个数比是5∶2,A错误;B、根据电子转移数相等,2个MnO4—得到10e-,则可氧化10个HCl分子,所以被氧化的盐酸占参加反应盐酸总分子数的5/8,B正确;C、KMnO4全部被还原为氯化锰,即高锰酸钾全部发生还原反应,C错误;D、根据以上分析可知KMnO4全部被还原,但HCl只有一部分发生氧化反应,D错误,答案选B。

【题目】磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1) 已知:25℃时,磷酸和氢氟酸的电离常数如下表所示。
物质 | H3PO4 | HF |
电离常数 | Ka1=7.1×10-3,Ka2=6.3×10-8, Ka1=4.2×10-13 | Ka=6.6×10-4 |
向 NaF 溶液中滴加少量 H3PO4溶液,反应的离子方程式为_____________。
(2) 已知:
Ⅰ.CaO(s)+H2SO4(l) ![]() CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1
CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1
Ⅱ.5CaO(s)+3H3PO4(l)+HF(g) ![]() Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1
Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1
则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为_____________。
②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率_______(填“ 增大”“ 减小”或“ 不变”,下同); HF的平衡浓度__________。
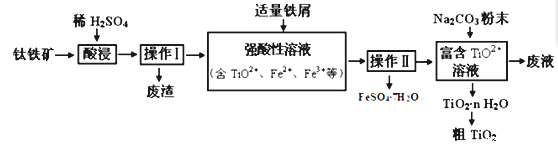
(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物 CO 可用于制备 H2,原理为
CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH。
CO2(g)+H2(g) ΔH。
①一定温度下,向 10 L 密闭容器中充入0.5 mol CO和 1 mol H2O(g),2 min 达到平衡时,测得 0~2 min 内用 CO2 表示的反应速率 v(CO2)=0.02 mol·L-1·min-1。则 CO的平衡转化率 α=________;该反应的平衡常数 K=______________。
②在压强不变的密闭容器中发生上述反应,设起始的![]() ,CO 的平衡体积分数(φ)与温度(T) 的关系如图所示。
,CO 的平衡体积分数(φ)与温度(T) 的关系如图所示。

则:该反应的 ΔH________0(填“>” “ <” 或“=”,下同)。 a______1,理由为_______________。