题目内容
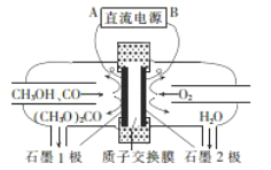
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇为主要原料制备环己烯。
已知: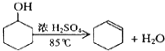
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 熔点(℃) | |
环乙醇 | 0.96 | 25 | 161 | 难溶于水 |
环乙烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____。
②试管C置于冰水浴中的目的是_____。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____层。(填上或下)
②再将环己烯按图2装置蒸馏,冷却水从口进入_____(填“g”或“f”)。收集产品时,控制的温度应在_____左右,实验制得的环己烯精品质量低于理论产量,最可能的原因是_____。
A.蒸馏时从70℃开始收集产品
B.环已醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
【答案】防暴沸 防止环己烯挥发 上 g ![]() c
c
【解析】
(1)①碎瓷片或者沸石的作用是防暴沸,故答案为:防暴沸;
②冰水浴的目的是降低环己烯蒸气的温度,使其液化,防止挥发,故答案为:防止环己烯挥发;
(2)①环己烯是烃类,不溶于氯化钠溶液,且密度比水小,振荡、静置、分层后环己烯在上层,故答案为:上;
②蒸馏操作中,冷凝水方向和蒸汽方向相反可提高冷凝效果,所以冷凝水从g口进入,根据表中数据可知,馏分环己烯的沸点为![]() ,故收集产品应控制温度在
,故收集产品应控制温度在![]() 左右;
左右; ![]() 蒸馏时从
蒸馏时从![]() 开始收集产品,提前收集,产品中混有杂质,实际产量高于理论产量,故a错误;
开始收集产品,提前收集,产品中混有杂质,实际产量高于理论产量,故a错误; ![]() 环己醇实际用量多了,制取的环己烯的物质的量增大,实验制得的环己烯精品质量高于理论产量,故b错误;
环己醇实际用量多了,制取的环己烯的物质的量增大,实验制得的环己烯精品质量高于理论产量,故b错误; ![]() 若粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量,故c正确;
若粗产品中混有环己醇,导致测定消耗的环己醇量增大,制得的环己烯精品质量低于理论产量,故c正确;
故答案为:g;![]() ;c。
;c。

【题目】下列有关化学实验操作,现象和结论均为正确的是
选项 | 操作 | 现象 | 结论 |
A | Mg2+和Cu2+共存的溶液中滴入适量NaOH溶液 | 产生白色沉淀 | 相同温度下,溶度积常数 Ksp[Mg(OH)2]<Ksp[Cu(OH)2] |
B | 加热盛有(NH4)2CO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 试纸变蓝 | (NH4)2CO3显碱性 |
C | 常温下,向等浓度、等体积的Na2CO3和NaHCO3溶液中滴加等量的酚酞溶液 | 碳酸钠溶液中红色更深 | 阴离子水解常数Kh: CO32->HCO3- |
D | 向饱和硼酸溶液中滴加少量Na2CO3粉末 | 无气泡冒出 | 不能证明酸性:碳酸>硼酸 |
A.AB.BC.CD.D