题目内容
【题目】25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是( )
A.向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c(Na+)c(NH4+)c(SO42-)c(OH-)c(H+)
B.0.1mol/LNaHC2O4溶液呈酸性:c(Na+)c(HC2O4-)c(H2C2O4)c(C2O42-)
C.20mL0.1mol/LCH3COONa溶液与10mL0.1mol/LHCl溶液混合后的酸性溶液:cCH3COOH2cH+c(CH3COO-)cOH-
D.浓度均为0.1mol/L的小苏打溶液与烧碱溶液等体积混合:c(Na+)c(H+)2c(CO32-)c(OH-)c(HCO3-)
【答案】D
【解析】
A.根据物料守恒可得:![]() ,则
,则![]() ;由于溶液为中性,则
;由于溶液为中性,则![]() ,根据电荷守恒可得:
,根据电荷守恒可得:![]()
![]() ,所以
,所以![]()
![]() ,结合
,结合![]() 可知:
可知:![]()
![]() ,所以溶液中离子浓度大小为:
,所以溶液中离子浓度大小为:![]() ,A错误;
,A错误;
B.![]() 溶液呈酸性,说明
溶液呈酸性,说明![]() 电离程度大于水解程度,所以
电离程度大于水解程度,所以![]() ,但是其电离和水解程度都较小,则存在
,但是其电离和水解程度都较小,则存在![]() ,B错误;
,B错误;
C.二者混合后,溶液中溶质为等物质的量浓度的![]() 、NaCl、
、NaCl、![]() ,溶液中存在电荷守恒
,溶液中存在电荷守恒![]() 、存在物料守恒
、存在物料守恒![]() ,所以存在
,所以存在![]() ,C错误;
,C错误;
D.等浓度、等体积的小苏打和烧碱溶液混合,二者恰好完全反应生成![]() ,溶液中存在电荷守恒,根据电荷守恒得
,溶液中存在电荷守恒,根据电荷守恒得![]() ,D正确。
,D正确。
答案选D。

 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
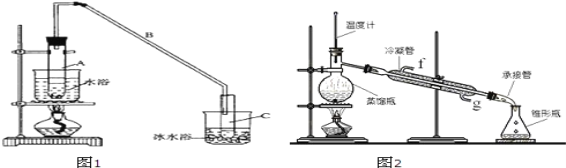
仁爱英语同步练习册系列答案【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇为主要原料制备环己烯。
已知: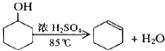
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 熔点(℃) | |
环乙醇 | 0.96 | 25 | 161 | 难溶于水 |
环乙烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____。
②试管C置于冰水浴中的目的是_____。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____层。(填上或下)
②再将环己烯按图2装置蒸馏,冷却水从口进入_____(填“g”或“f”)。收集产品时,控制的温度应在_____左右,实验制得的环己烯精品质量低于理论产量,最可能的原因是_____。
A.蒸馏时从70℃开始收集产品
B.环已醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 在0.1 molL-1Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深 | CO32-水解是吸热反应 |
B | 等体积、pH=3的两种酸HA和HB分别与足量的Zn反应,酸HA放出的氢气多 | 酸性A比B强 |
C | 常温下,用饱和Na2CO3溶液可将BaSO4部分转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
D | 室温下,用pH试纸测得:0.1 molL-1 Na2SO3溶液的pH约为10;0.1 molL-1 NaHSO3溶液的pH约为5 | HSO |
A. A B. B C. C D. D