题目内容
【题目】下列说法中,正确的是( )
A.![]() 与
与![]() 互为同系物
互为同系物
B.分子组成为C4H8O2,其中属于酯的结构有4种
C.乙醇和乙醚互为同分异构体
D.具有相同的分子通式的有机物一定是同系物
【答案】B
【解析】
A.![]() 属于酚,
属于酚,![]() 属于醇,结构不相似,不是同系物,故A错误;
属于醇,结构不相似,不是同系物,故A错误;
B.分子组成为C4H8O2,其中属于酯的结构有4种,HCOOCH2CH2CH3 甲酸正丙酯、COOCH(CH3)2 甲酸异丙酯、CH3COOCH2CH3 乙酸乙酯、CH3CH2COOCH3 丙酸甲酯,故B正确;
C.乙醇分子式为C2H6O,乙醚分子式为C4H10O,两者分子式不同,不是同分异构体,故C错误;
D.具有相同的分子通式的有机物不一定是同系物,如烯烃和环烷烃,故D错误;
故选B。

【题目】直接排放含SO2的烟气会形成酸雨危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应原理为__。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式为__。
(3)吸收液吸收SO2的过程中,pH随n(![]() ):n(
):n(![]() )变化关系如表:
)变化关系如表:
n( | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显性__(填“酸”或“碱”),用化学平衡原理解释__。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(填字母编号)__。
a.c(Na+)=2c(![]() )+c(
)+c(![]() )
)
b.c(Na+)>c(![]() )>c(
)>c(![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
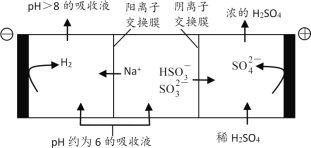
①![]() 在阳极放电的电极反应式是__。
在阳极放电的电极反应式是__。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理__。
【题目】已知某溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、![]() 、
、![]() 、
、![]() 、I-、
、I-、![]() 、
、![]() 中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
(1)根据下列实验步骤和现象,推断实验结论:
实验步骤与实验现象 | 实验结论 |
Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是____。 |
Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是_____,一定含有的离子是____。 |
Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是____,生成沉淀A的离子方程式为____。 |
Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有___,可能含有____。 |
(2)上述实验步骤Ⅳ中开始阶段一定发生的离子方程式是______。
(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示。
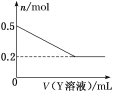
Y可能为(填化学式)____,B的组成为______。