题目内容
11.四氯化碳按官能团分类应该属于( )| A. | 烷烃 | B. | 烯烃 | C. | 卤代烃 | D. | 炔烃 |
分析 四氯化碳中含-Cl,为卤代烃的官能团,以此来解答.
解答 解:A.烷烃中不含官能团,故A不选;
B.烯烃的官能团为碳碳双键,故B不选;
C.卤代烃的官能团为卤素原子,则四氯化碳属于卤代烃,故C选;
D.炔烃的官能团为碳碳三键,故D不选;
故选C.
点评 本题考查有机物的官能团及分类,注意把握常见有机物的官能团即可解答,注重基础知识的考查,题目较简单.

练习册系列答案
相关题目
9.标准状况下有①0.112L水;②3.01×1023个氯化氢分子;③13.6g H2S气体;④0.2mol氨气,下列对这四种物质的关系由小到大排列正确的是( )
| A. | 体积:④③②① | B. | 密度:④①③② | C. | 质量:①④③② | D. | 氢原子数:②④③① |
2.下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
①氨基酸 ②蛋白质 ③Al(OH)3 ④Al2O3 ⑤AlCl3 ⑥Al.
| A. | 除②以外 | B. | 除⑤以外 | C. | 除⑥以外 | D. | 全部 |
19.W、X、Y、Z是短周期元素,它们的核电荷数依次增大.下表列出它们的性质和结构:
(1)元素符号:XO,ZNa.
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式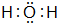 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
| 元素编号 | 元素性质或原子结构 |
| W | 原子电子层数与核外电子数相等 |
| X | 核外S能级上的电子总数与P能级上的电子总数相等 |
| Y | 元素的原子半径在该周期中最大(除稀有气体外) |
| Z | 原子核外P能级上的电子总数比S能级上的电子总数多2 |
(2)Y元素原子的核外最外层电子排布式为3s1.
(3)W和X形成的化合物的电子式
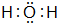 ,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
,该化合物为极性分子(填“极性”或“非极性”).Z和X形成的化合物构成的晶体属于原子晶体.
16.在同温同压下,下列各组热化学方程式中,△H2>△H 1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g),△H 1;2H2(g)+O2(g)=2H2O(l),△H2 | |
| B. | S(g)+O2(g)=SO2(g),△H 1;S(s)+O2(g)=SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g),△H 1;C(s)+O2(g)=CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g),△H 1;2H2(g)+2Cl2(g)=4HCl(g)△H2 |
3.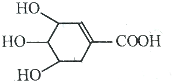 八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图所示.下列关于莽草酸的说法错误的是( )
八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图所示.下列关于莽草酸的说法错误的是( )
 八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图所示.下列关于莽草酸的说法错误的是( )
八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构如图所示.下列关于莽草酸的说法错误的是( )| A. | 可以通过加成反应或取代反应生成含有卤原子的产物 | |
| B. | 含有7种氢原子 | |
| C. | 1mol莽草酸与足量金属钠反应可以得到2mol氢气 | |
| D. | 能发生酯化反应,也能发生消去反应 |
20.室温时,下列溶液混合后,pH大于7的是( )
| A. | 0.1mol/L的盐酸和pH=13的氢氧化钡溶液等体积混合 | |
| B. | 0.1mol/L的NaHCO3溶液和pH=1的盐酸等体积混合 | |
| C. | pH=3的硫酸和pH=11的氨水等体积混合 | |
| D. | pH=1的醋酸和0.1mol/L的氢氧化钠溶液等体积混合 |