题目内容
17.如图所示,A、B中电极为多孔惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极.若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中.切断K1,闭合K2、K3通直流电,通电一段时间后,状态如图所示,则:(提示:注意观察试管中的气体体积比)
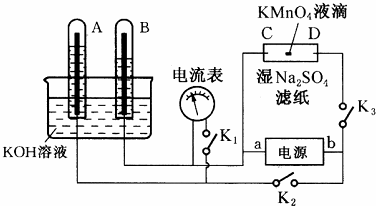
(1)电源a为负极.
(2)在湿的Na2SO4滤纸条中心的KMnO4液滴,有什么现象紫色向D方向移动.
(3)A极的电极反应式是4OH--4e-=O2↑+2H2O.
(4)一段时间后,KOH溶液pH值增大(填“增大”、“减小”或“不变”).
若A、B中均有气体包围电极.此时切断K2、K3,闭合K1,电流表的指针偏转,则此时A极电极反应式为O2+2H2O+4e-=4OH-.
分析 电解KOH溶液时,阳极上生成氧气、阴极上生成氢气,且氧气和氢气体积之比为1:2,根据图知,A中气体是氧气、B中气体是氢气,则A中电极为阳极、B中电极为阴极;
(1)连接阳极的电极是正极、连接阴极的电极是负极;
(2)高锰酸钾溶液中高锰酸根离子呈红色,电解过程中,阳离子向阴极移动、阴离子向阳极移动;
(3)A电极上氢氧根离子放电生成氧气;
(4)电解KOH溶液时,实际上是电解水,KOH不参加反应,所以KOH的物质的量不变,水的量减少,导致KOH浓度增大;
若A、B中均有气体包围电极,此时切断K2、K3,闭合K1,电流表的指针偏转,说明构成原电池,有氢气的电极是负极、有氧气的电极是正极,正极上氧气得电子和水反应生成氢氧根离子.
解答 解:电解KOH溶液时,阳极上生成氧气、阴极上生成氢气,且氧气和氢气体积之比为1:2,根据图知,A中气体是氧气、B中气体是氢气,则A中电极为阳极、B中电极为阴极;
(1)连接阳极的电极是正极、连接阴极的电极是负极,a连接阴极,则a是负极,故答案为:负;
(2)高锰酸钾溶液中高锰酸根离子呈红色,电解过程中,阳离子向阴极移动、阴离子向阳极移动,电解时,硫酸钠溶液和铂电极构成电解池,C是阴极、D是阳极,所以高锰酸根离子向阳极D电极移动,则看到的现象是紫色向D方向移动,故答案为:紫色向D方向移动;
(3)A电极上氢氧根离子放电生成氧气,电极反应式为4OH--4e-=O2↑+2H2O,故答案为:4OH--4e-=O2↑+2H2O;
(4)电解KOH溶液时,实际上是电解水,KOH不参加反应,所以KOH的物质的量不变,水的量减少,导致KOH浓度增大,所以溶液的pH增大;
若A、B中均有气体包围电极,此时切断K2、K3,闭合K1,电流表的指针偏转,说明构成原电池,有氢气的电极是负极、有氧气的电极是正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为O2+2H2O+4e-=4 OH-,故答案为:增大;O2+2H2O+4e-=4 OH-.
点评 本题考查原电池和电解池原理,为高频考点,正确判断正负极、阴阳极是解本题关键,知道各个电极上发生的反应,难点是电极反应式的书写,题目难度不大.

| A. | CH4+Cl2→CH3Cl+HCl | B. | CH2=CH2+H2O→CH3CH2OH | ||
| C. |  +HO-NO2→ +HO-NO2→ +H2O +H2O | D. | CH3CH2OH→CH2=CH2+H2O |
| A. | 将等物质的量的CH4和Cl2在光照下反应生成纯净的CH3Cl | |
| B. | 将苯与浓硝酸和浓硫酸混合水浴加热制取硝基苯 | |
| C. | 用新制Cu(OH)2悬浊液鉴别葡萄糖和蔗糖 | |
| D. | 用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
| A. | R的最高价氧化物为RO3 | B. | R一定是第ⅦA族元素 | ||
| C. | R的气态氢化物能燃烧 | D. | R的气态氢化物易溶于水显碱性 |
 ,而不排布成
,而不排布成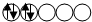 ,其直接的根据是洪特规则.
,其直接的根据是洪特规则.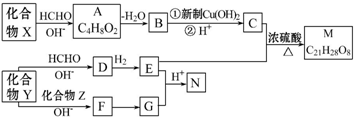
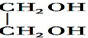 $\stackrel{H+}{→}$
$\stackrel{H+}{→}$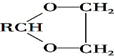 +H2O
+H2O
 .
.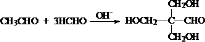 .
.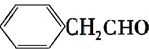
 .
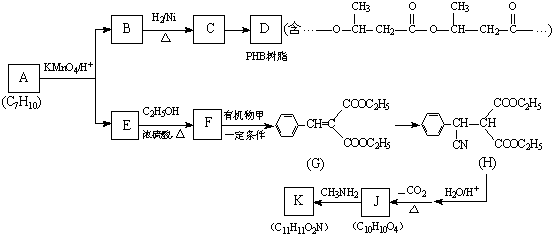
.
 $\stackrel{KMnO4/H+}{→}$RCOOH+
$\stackrel{KMnO4/H+}{→}$RCOOH+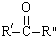
 +H2O
+H2O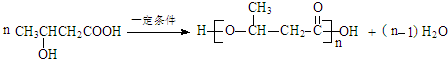 .
.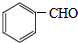 .
. .
.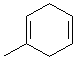 .
.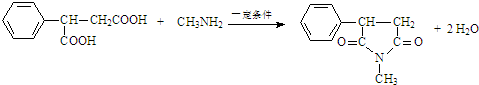 .
.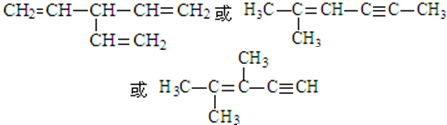 (写出一种即可).
(写出一种即可).