题目内容
7.写出下列物质的结构式(CN)2N≡C-C≡N HClOH-O-Cl S2Cl2Cl-S-S-Cl.
分析 (CN)2为共价化合物,1个分子中存在2个碳氮三键,1个碳碳单键,据此书写结构式;
HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,据此书写结构式;
S2Cl2的结构与双氧水类似,根据类比双氧水的结构进行判断.
解答 解:碳最外层为4个电子,氮原子最外层为5个电子,(CN)2为共价化合物,各原子满足8电子结构,所以1个分子中存在2个碳氮三键,1个碳碳单键,其结构式为:N≡C-C≡N,
HClO为共价化合物,分子中存在1个氧氢键和1个Cl-O键,次氯酸的电子式为: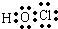 ,结构式为:H-O-Cl,
,结构式为:H-O-Cl,
S2Cl2分子中氯原子与硫原子之间形成1对共用电子对,硫原子与硫原子之间形成1对共用电子对,所以其结构式为:Cl-S-S-Cl,
故答案为:N≡C-C≡N;H-O-Cl;Cl-S-S-Cl.
点评 本题考查了结构式的书写,题目难度不大,充分考查了学生对书写知识的掌握情况,试题有利于培养学生灵活应用所学知识的能力,注意不常见的物质(CN)2根据各原子满足8电子结构书写.

练习册系列答案
相关题目
2.下列反应中反应物的总能量比生成物低的是( )
| A. | 镁与二氧化碳反应 | |
| B. | 铁和稀硫酸的反应 | |
| C. | 氢氧化钡晶体的粉末和氯化铵晶体混合 | |
| D. | 木炭在氧气中燃烧 |
16.1932年美国化学家鲍林(L.Pauling)首先提出了电负性的概念.如表给出的是第三周期的七种元素和第四周期的钾元素的电负性的值:运用表中数据解答,估计钙元素的电负性的取值范围( )
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
| A. | 小于0.8 | B. | 大于1.2 | C. | 在0.8与1.2之间 | D. | 在0.8与1.5之间 |
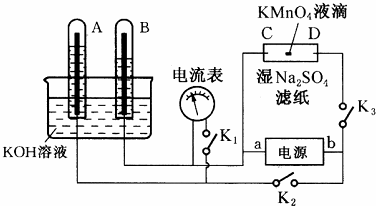
 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:(RCH3CH=CH2+HCl$\stackrel{催化剂}{→}$RCH3CHClCH3)
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:(RCH3CH=CH2+HCl$\stackrel{催化剂}{→}$RCH3CHClCH3)  实验室制取乙烯的装置如下图所示,请回答:
实验室制取乙烯的装置如下图所示,请回答: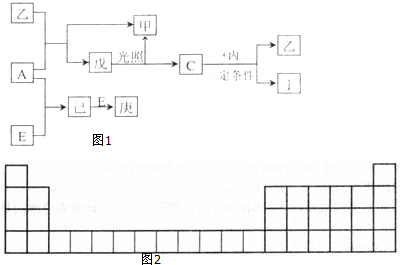
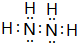 .
.