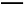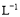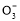题目内容
下表是五种银盐的溶度积常数(25 ℃):
化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法不正确的是( )
A.五种物质在常温下Ag2SO4饱和溶液中c(Ag+)最大
B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀
C.对于氯化银、溴化银和碘化银三种物质在常温下的饱和溶液中c(Ag+)随着氯、溴、碘的顺序增大
D.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
C
【解析】由溶度积的数据可知:AgCl、AgBr、AgI三种物质在常温下的饱和溶液中c(Ag+)随着氯、溴、碘的顺序而减小,C错误,又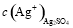 =
= 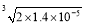 mol·L-1>c(Ag+)AgCl=
mol·L-1>c(Ag+)AgCl=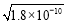 mol·L-1,结合前面所述,A正确;由于Ksp(Ag2S)?Ksp(AgCl),将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀,B正确;溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动,D正确。
mol·L-1,结合前面所述,A正确;由于Ksp(Ag2S)?Ksp(AgCl),将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀,B正确;溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动,D正确。

发酵粉是一种化学膨松剂,可由小苏打、臭粉(碳酸氢铵)、明矾中的两种物质组成。某小组为探究不同品牌的发酵粉的化学成分,进行如下实验。
【提出假设】
(1)假设1:由小苏打和臭粉组成
假设2:由小苏打和明矾组成
假设3:由 组成
【方案与流程】
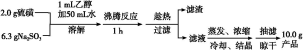
为探究甲品牌的发酵粉的成分,某同学设计如下实验,得到如下现象:
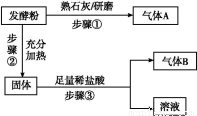
(2)结合步骤①~③分析,气体A为 ,该发酵粉的成分为 (填化学式)。
(3)若步骤①和②操作不变(现象也相同),将步骤③中足量稀盐酸改为足量氯化钡溶液,观察到有白色沉淀生成,能否确定发酵粉的成分并说明理由: 。
(4)乙品牌的发酵粉的化学组成可能为假设2情况,请你设计实验验证。
实验仪器和用品任选,限选试剂:稀盐酸、0.1 mol/L NaOH溶液
写出实验步骤、预期现象和结论。
实验步骤 | 预期现象和结论 |
步骤1:取少量样品溶于足量的盐酸后,将溶液分成两份,分别装入A、B试管中 |
|
步骤2:
| ,证明有Na+,发酵粉中有NaHCO3 |
步骤3:
| ,结合步骤2中的结论,假设2成立 |
常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如表所示:
实验编号 | HA的物质的 量浓度(mol·L-1) | NaOH的物质的 量浓度(mol·L-1) | 混合后溶 液的pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.12 | 0.1 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?
(2)乙组混合溶液中离子浓度c(A-)和c(Na+)的大小关系是 。
A.前者大 B.后者大 C.两者相等D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 。
(4)分析丁组实验数据,写出该混合溶液中下列算式的精确结果(列式):
c(Na+)-c(A-)= mol·L-1。