题目内容
【题目】已知H2(g)+Cl2(g)=2HCl(g) ΔH= -184.6kJ/mol,则![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g)的ΔH为( )
Cl2(g)=HCl(g)的ΔH为( )
A.+184.6kJ/molB.-92.3kJ/molC.-369.2kJ/molD.+92.3kJ/mol
【答案】B
【解析】
热化学方程式是表示参加反应物质的量与反应热的关系的化学方程式,书写和应用热化学方程式时必须注意各物质化学式前的化学计量数可以是整数,也可以是分数;反应热与反应方程式相互对应,若反应式的书写形式不同,相应的化学计量数不同,则反应热亦不同;反应方向改变,焓变数值符号改变。
依据热化学方程式的书写原则和方法,已知H2(g)+Cl2(g)=2HCl(g) ΔH= -184.6kJ/mol,化学方程式的系数除以2,则焓变也应除以2,得到热化学方程式![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl(g) ΔH= -92.3kJ/mol。
Cl2(g)=HCl(g) ΔH= -92.3kJ/mol。
答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= __________,已知:K3000C>K3500C,则该反应是______热反应。
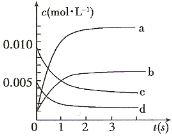
(2)图中表示NO2的变化的曲线是_____________;用O2表示从0~2 s内该反应的平均速率v=____________
(3)能说明该反应已达到平衡状态的是____________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是____________
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)关于该反应的下列说法中,正确的是________(填字母)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0