题目内容
【题目】NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有NA个H2O分子
B.常温常压下,22.4LCO2中碳原子数大于NA个
C.1L1mol·L-1的稀硝酸中,含氧原子数大于3NA
D.0.1mol/L Na2SO4溶液含Na+离子数为0.2NA个
【答案】C
【解析】
A. 标准状况下,H2O为液体,无法用气体摩尔体积计算其物质的量,A错误;
B. 常温常压下,22.4LCO2中碳原子数小于NA个,B错误;
C. 1L1mol·L-1的稀硝酸中,水中也含有氧原子,则含氧原子数大于3NA,C正确;
D. 0.1mol/L Na2SO4溶液未给定体积,则含Na+离子数无法计算,D错误;
答案为C。

练习册系列答案
相关题目
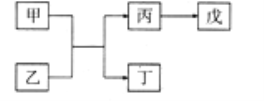
【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
反应装置或图像 | 实验现象或图像信息 | |
A |
| 反应开始后,针筒活塞向右移动 |
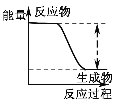
B |
| 反应物总能量大于生成物总能量 |
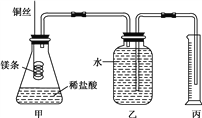
C |
| 反应开始后,甲处液面低于乙处液面 |
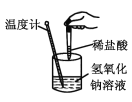
D |
| 温度计的水银柱不断上升 |
A. AB. BC. CD. D