��Ŀ����
(10��)��һ���¶��£���2molA��2molB�����������Ϻ����ݻ�Ϊ2L��ij�ܱ������У��������·�Ӧ3A(g)+B(g)  xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
��1��xֵ����________________
��2��A��ת����Ϊ_________________
��3������D�ķ�Ӧ����Ϊ_________________
��4���������Ӧ��ϵ��ѹǿ����ƽ����ϵ��C����������_________(����С������)
��5�����������Ӧ����ͬ�����´��淴Ӧ��ʼ���У���ʼ����C��D��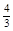 mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol
mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol
 xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף�
xC(g)+2D(g)��2minĩ��Ӧ�ﵽƽ��״̬��������0.8molD�������C��Ũ��Ϊ0.4mol/L������д���пհף���1��xֵ����________________
��2��A��ת����Ϊ_________________
��3������D�ķ�Ӧ����Ϊ_________________
��4���������Ӧ��ϵ��ѹǿ����ƽ����ϵ��C����������_________(����С������)
��5�����������Ӧ����ͬ�����´��淴Ӧ��ʼ���У���ʼ����C��D��
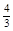 mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol
mol��Ҫʹƽ��ʱ�����ʵ�����������ԭƽ��ʱ��ȫ��ȣ���Ӧ����________����_________mol(10��)ÿ��2�� (1)2 (2)60% (3)0.2 mol/(L?min) (4) ���䣨5��B 4/3
������淴Ӧ���йؼ��㡣
��1��ƽ��ʱ����C�����ʵ�����1.4mol/L��2L��0.8mol�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪��x��2��
��2�����ݷ���ʽ��֪������0.8molD��������A��1.2mol������A��ת������1.2��2��100����60����
��3����Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������D�ķ�Ӧ������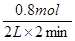 ��)0.2 mol/(L?min)��
��)0.2 mol/(L?min)��
��4�����ݷ���ʽ��֪�����ڷ�Ӧǰ������Dz���ģ����Ըı�ѹǿƽ���Dz��ƶ��ģ����C�ĺ����Dz���ġ�
��5��Ҫ����ƽ���Ч������ݷ���ʽ����֮��A��B�����ʵ�������������ʵ���Ӧ������ȵģ�����C��D����4/3mol�����ݷ���ʽ��֪�����൱��A��2mol��B��2/3mol�����Ի���Ҫ�ڼ���2mol��2/3mol��4/3mol��B���ʡ�
��1��ƽ��ʱ����C�����ʵ�����1.4mol/L��2L��0.8mol�����ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪��x��2��
��2�����ݷ���ʽ��֪������0.8molD��������A��1.2mol������A��ת������1.2��2��100����60����
��3����Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������D�ķ�Ӧ������
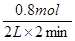 ��)0.2 mol/(L?min)��
��)0.2 mol/(L?min)����4�����ݷ���ʽ��֪�����ڷ�Ӧǰ������Dz���ģ����Ըı�ѹǿƽ���Dz��ƶ��ģ����C�ĺ����Dz���ġ�
��5��Ҫ����ƽ���Ч������ݷ���ʽ����֮��A��B�����ʵ�������������ʵ���Ӧ������ȵģ�����C��D����4/3mol�����ݷ���ʽ��֪�����൱��A��2mol��B��2/3mol�����Ի���Ҫ�ڼ���2mol��2/3mol��4/3mol��B���ʡ�

��ϰ��ϵ�д�
�����Ŀ
 x C(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L���ݴ���д���¿հף�
x C(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L���ݴ���д���¿հף� CH3COCH2COH(CH3)2(l)�� ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ���ߣ�Y��t������ͼ��ʾ������˵����ȷ����
CH3COCH2COH(CH3)2(l)�� ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ���ߣ�Y��t������ͼ��ʾ������˵����ȷ����
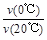 >1
>1 =1
=1 2Z��g���˷�Ӧ�ﵽƽ��ı�־��
2Z��g���˷�Ӧ�ﵽƽ��ı�־�� 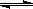 N2O4 (g)��
N2O4 (g)��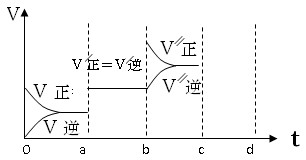
 2C(g) ��H ��0�����и�ͼ����ȷ����
2C(g) ��H ��0�����и�ͼ����ȷ����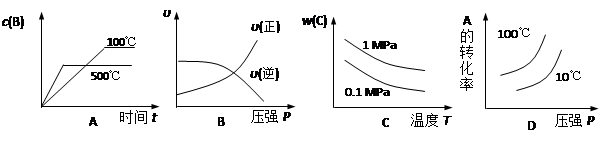
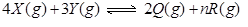 ����ƽ����������¶Ȳ��䣬ƽ���ѹǿ��ԭ������5����X��Ũ�ȼ�С����÷�Ӧ����ʽ�е�nֵ�ǣ� ��
����ƽ����������¶Ȳ��䣬ƽ���ѹǿ��ԭ������5����X��Ũ�ȼ�С����÷�Ӧ����ʽ�е�nֵ�ǣ� �� pC��g���ﵽƽ������¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1��9��������˵������ȷ���ǣ� ��
pC��g���ﵽƽ������¶Ȳ��䣬�����������С��ԭ����1/2�����ﵽ��ƽ��ʱ��C��Ũ��Ϊԭ����1��9��������˵������ȷ���ǣ� ��