题目内容
15.NA为阿伏加德罗常数的值,下列说法一定正确的是( )| A. | 1 L 1 mol•L-1的醋酸溶液中含有的醋酸分子数为NA | |
| B. | 电解精炼铜时,当阳极上质量减少6.4 g时,电路中转移的电子数为2NA | |
| C. | 常温下,46 g NO2和N2O4的混合物中含有的氧原子数为2NA | |
| D. | 11.2 L CO2中含有的分子数为0.5NA |
分析 A、醋酸是弱电解质,在溶液中部分电离;
B、活泼金属优先在阳极上失去电子,粗铜中铁锌等杂质摩尔质量小,6.4g金属失去的电子大于0.2mol;
C、NO2和N2O4的最简式均为NO2;
D、气体所处的状态不明确.
解答 解:A、醋酸是弱电解质,在溶液中部分电离,故溶液中含有的醋酸分子的物质的量小于1mol,即小于NA个,故A错误;
B、电解精炼铜时,活泼金属优先在阳极上失去电子,粗铜中铁、锌等杂质摩尔质量小于铜的,6.4g金属失去的电子大于0.2mol,转移的电子数目大于0.2 NA,故B错误;
C、NO2和N2O4的最简式均为NO2,故4.6g混合气体中含有NO2的物质的量n=$\frac{4.6g}{46g/mol}$=0.1mol,故含有0.2mol氧原子,即0.2NA个,故C正确;
D、气体所处的状态不明确,不一定是标况,不能根据气体摩尔体积来计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
5.H、N、O、P、Cr、Fe是元素周期表中六种常见元素.
(1)P位于元素周期表第三周期第ⅤA族;Cr的基态原子价层电子排布式是3d54s1.O的一种18电子结构氢化物的电子式是 .
.
(2)用“>”“<”填空:
(3)以铁作阳极,利用电解生成的Fe2+而将酸性含铬废水(K2Cr2O7)中的铬元素还原为三价,之后电解沉淀而除去,写出前一步反应的离子方程式:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
(4)已知:
3Fe(s)+2O2(g)=Fe3O4(s)△H=-1118.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-438.6kJ/mol,
则3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)的△H=-151.2KJ/mol.
(1)P位于元素周期表第三周期第ⅤA族;Cr的基态原子价层电子排布式是3d54s1.O的一种18电子结构氢化物的电子式是
 .
.(2)用“>”“<”填空:
| 电负性 | 熔沸点 | 稳定性 | 酸性 |
| O>N | NH3>PH3 | Fe2+< Fe3+ | H3PO4<HNO3 |
(4)已知:
3Fe(s)+2O2(g)=Fe3O4(s)△H=-1118.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-438.6kJ/mol,
则3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)的△H=-151.2KJ/mol.
6.下列说法或表示方法正确的是( )
| A. | 已知Ka(HCN)<Ka(CH3COOH),当物质的量浓度相同时,CH3COOH中水电离出c(H+)大于HCN中水电离出的c(H+) | |
| B. | 由C(石墨)=C(金刚石)△H=+1.90 kJ•mol-1可知,金刚石比石墨稳定 | |
| C. | 向2.0 mL浓度均为0.1 mol•L-1 的KCl、KI混合溶液中滴加1~2滴0.01 mol•L-1 AgNO3 溶液,振荡,沉淀呈黄色,说明AgCl 的Ksp比AgI 的Ksp大 | |
| D. | 在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧热的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ•mol-1 |
10.某有机物的结构简式如图所示,下列有关该有机物的说法正确的是( )
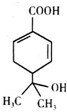

| A. | 分子式为C10H13O3 | |
| B. | 含有两种官能团,可使溴水和酸性高锰酸钾溶液褪色 | |
| C. | 能发生加成、取代、氧化等反应 | |
| D. | 与钠和氢氧化钠溶液都能发生反应,且得到的产物相同 |
5.下列关于物质或离子检验的叙述正确的是( )
| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ | |
| D. | 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |


