题目内容
【题目】“探险队员”﹣盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过.
(1)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有个,属于氧化还原反应的有个,其中能“吃掉”盐酸的盐是(填化学式),写出该反应的离子方程式 .
(2)在不能与盐酸反应的物质中,属于电解质的是(填写物质序号,下同),属于非电解质的是 .
(3)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线) .
【答案】
(1)2,1,Na2CO3,CO32﹣+2H+=CO2↑+H2O
(2)⑥?,③⑩
(3)③→⑥→⑩→⑦→?→?
【解析】解:(1)中和反应是酸与碱反应,根据碱的种类确定中和反应的个数,碱有2种,则中和反应有2个;能与盐酸反应化合价发生变化的只有锌,则发生的氧化还原反应只有1个;能与盐酸反应的盐只有Na2CO3,碳酸钠和盐酸都属于强电解质,在溶液中完全电离,反应生成二氧化碳气体和水,反应的化学方程式为Na2CO3+2HCl═2NaCl+CO2↑+H2O,反应的离子方程式为CO32﹣+2H+=CO2↑+H2O,
所以答案是:2;1;Na2CO3;CO32﹣+2H+=CO2↑+H2O;
(2)与盐酸不反应的有二氧化碳、不活泼金属铜和银、氯化钠、二氧化硫、硫酸,
二氧化碳和二氧化硫自身不能电离,属于非电解质;
铜和银是金属单质,既不是电解质也不是非电解质;
氯化钠在水溶液中或熔融状态下能够导电,属于电解质;
硫酸在水溶液中能够导电,属于电解质;
故属于电解质的是:⑥氯化钠,硫酸;属于非电解质的是:③二氧化碳,⑩二氧化硫,
所以答案是:⑥;③⑩;
(3)利用图示的物质对相关的与盐酸不能反应的物质作出判断即可,由于盐酸不能和二氧化碳、二氧化硫、硫酸、铜、银等反应,走出迷宫所走的路线为③→⑥→⑩→⑦→→,
所以答案是:③→⑥→⑩→⑦→→.

【题目】按要求写出方程式.
(1)碳酸氢铵溶液中加入过NaOH溶液,并加热(写出离子方量程式) .
(2)已知4℃时四种化合物在水中和液氨中的溶解度如表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O (液) | 170g | 9.2g | 1.5×10﹣4g | 33.3g |
NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为 , 在液氨中发生复分解反应的化学方程式为 .
【题目】如图a、b、c、d均为铂电极,供选择的电解质溶液如下表:
组 | A | B | C | D |
甲槽 | NaOH | Cu(N O3)2 | KCl | Na2SO4 |
乙槽 | CuSO4 | NaCl | AgNO3 | NaNO3 |
要满足的条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等.则应选用的电解液是( )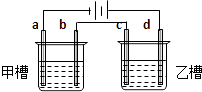
A.A
B.B
C.C
D.D