题目内容
【题目】根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式:
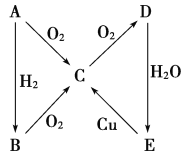
(1)当A为气体单质时,A是________,B是__________,C是________,D是________,E是________,E→C的化学方程式:_________________________________________________。
(2)当A为固体单质时,A是________,B是________,C是________,D是________,E是________,E→C的化学方程式是_______________________________________________。
【答案】N2 NH3 NO NO2 HNO3 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O S H2S SO2 SO3 H2SO4 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
【解析】
(1)当A是气体单质时,A能与氧气、氢气反应,且B能发生连续氧化反应,E能和Cu反应生成C,则E为硝酸,所以A是N2,B为NH3,C为NO,D为NO2,E为HNO3;据以上分析解答。
(2)如果A是固体单质,E为酸,能和Cu反应生成C,则E是硫酸, A是S,B是H2S,C是SO2,D是SO3, E是H2SO4;据此分析解答。
(1)当A是气体单质时,A能与氧气、氢气反应,且B能发生连续氧化反应,E能和Cu反应生成C,则E为硝酸,A为氮气,A和氢气反应生成B为氨气,A和氧气反应生成C为NO, NO被氧气氧化生成D为二氧化氮,二氧化氮和水反应生成硝酸E,所以当A为气体单质时,A是N2,B为NH3,C为NO,D为NO2,E为HNO3;稀硝酸和铜反应生成一氧化氮、硝酸铜和水,E→C的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O;
综上所述,本题答案是:N2,NH3,NO,NO2,HNO3;3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(2)如果A是固体单质,E为酸,能和Cu反应生成C,则E是浓硫酸,则A为S,A和氢气反应生成B为H2S,A和氧气反应生成C为SO2,C被氧气氧化生成D为SO3;当A为固体单质时,A是S,B是H2S,C是SO2,D是SO3, E是H2SO4;浓硫酸和铜加热反应生成硫酸铜、二氧化硫和水,E→C的化学方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
综上所述,本题答案是:S, H2S, SO2, SO3, H2SO4;Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。

【题目】某小组通过分析镁与酸反应时pH的变化,探究镁与醋酸溶液反应的实质。
(实验)在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1 g光亮的镁屑(过量)放入10 mL 0.10 mol·L–1 HCl溶液中;
Ⅱ.取0.1 g光亮的镁屑放入10 mL 0.10 mol·L–1 CH3COOH溶液(pH = 2.9)中;
Ⅲ.取0.1 g光亮的镁屑放入10 mL pH = 2.9 HCl溶液中。
(数据)
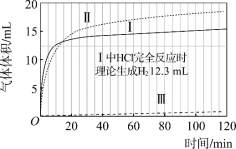
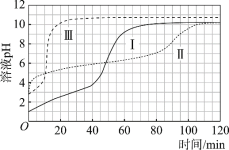
图1 图2
(1)起始阶段,Ⅰ中主要反应的离子方程式是____。
(2)Ⅱ起始溶液中![]() 约为____。(选填“1”、“10”或“102”)
约为____。(选填“1”、“10”或“102”)
(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是c(H+),实验证据是____。
(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设:CH3COOH能直接与Mg反应。
进行实验Ⅳ:____。
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10 mol·L–1的 CH3COOH与0.10 mol·L–1 CH3COONa的混合溶液(pH = 4.8),气体产生速率与Ⅱ对比如下。
a.实验Ⅴ起始速率 | b.实验Ⅱ起始速率 | c.实验ⅡpH=4.8时速率 |
2.1 mL·min–1 | 2.3 mL·min–1 | 0.8 mL·min–1 |
对比a~c中的微粒浓度,解释其a与b、a与c气体产生速率差异的原因:____。
(6)综合以上实验得出结论:
①镁与醋酸溶液反应时,CH3COOH、H+、H2O均能与镁反应产生氢气;
②____。
(7)实验反思:120 min附近,Ⅰ~ⅢpH均基本不变,pH(Ⅰ) ≈ pH(Ⅱ) < pH(Ⅲ),解释其原因:____。