题目内容
(10分)制取碘盐的流程如下:

试回答下列问题
(1)检验母液中是否含有SO42-离子的方法是 ▲ 。
(2)过滤时,用到的玻璃仪器有: ▲ 、 ▲ 、 ▲ 。
(3)国家标准GB546061-92规定碘盐含碘量(以碘计),出厂产品≥40mg/Kg。销售品≥30mg/Kg。某次实验时向一干净的坩埚中放入5g精盐,加入1mL0.001mol/L标准KIO3溶液搅拌均匀,在100℃恒温烘干1h,即得碘盐产品,该碘盐的含碘量约为: ▲ mg/Kg(保留一位小数),是否是合格产品 ▲ (填:合格、不合格)。
(4)检验碘盐是否加有碘酸钾,定性检验方法是在酸性介质中加还原剂KCNS,其反应如下:6IO3-+5CNS-+H++2H2O=3I2+5HCN+5SO42-,检验时,除需用KCNS外,还需要的一种试剂,最好是 ▲ 。
(5)碘盐中的碘酸钾在560℃开始分解产生无色气体,剩余固体加硝酸酸化的硝酸银有黄色沉淀,碘盐在热水中,也会生成两种单质,其中一种是无色气体,滴加酚酞显红色,请写出碘酸钾两种情况下分解的化学方程式: ▲ 或 ▲ 。

试回答下列问题
(1)检验母液中是否含有SO42-离子的方法是 ▲ 。
(2)过滤时,用到的玻璃仪器有: ▲ 、 ▲ 、 ▲ 。
(3)国家标准GB546061-92规定碘盐含碘量(以碘计),出厂产品≥40mg/Kg。销售品≥30mg/Kg。某次实验时向一干净的坩埚中放入5g精盐,加入1mL0.001mol/L标准KIO3溶液搅拌均匀,在100℃恒温烘干1h,即得碘盐产品,该碘盐的含碘量约为: ▲ mg/Kg(保留一位小数),是否是合格产品 ▲ (填:合格、不合格)。
(4)检验碘盐是否加有碘酸钾,定性检验方法是在酸性介质中加还原剂KCNS,其反应如下:6IO3-+5CNS-+H++2H2O=3I2+5HCN+5SO42-,检验时,除需用KCNS外,还需要的一种试剂,最好是 ▲ 。
(5)碘盐中的碘酸钾在560℃开始分解产生无色气体,剩余固体加硝酸酸化的硝酸银有黄色沉淀,碘盐在热水中,也会生成两种单质,其中一种是无色气体,滴加酚酞显红色,请写出碘酸钾两种情况下分解的化学方程式: ▲ 或 ▲ 。
(1)取少量母液先加入稀盐酸酸化,再加入BaCl2溶液,若有白色沉淀,则说明有SO42-离子。
(2)漏斗 玻璃棒 烧杯
(3)25.4 不合格
(4)淀粉溶液
(5)2KIO3 2KI+3O2↑ 12KIO3+6H2O
2KI+3O2↑ 12KIO3+6H2O 6I2+12KOH+15O2↑
6I2+12KOH+15O2↑
(第3小题第一小问2分,其它每空1分,共10分)
(2)漏斗 玻璃棒 烧杯
(3)25.4 不合格
(4)淀粉溶液
(5)2KIO3
 2KI+3O2↑ 12KIO3+6H2O
2KI+3O2↑ 12KIO3+6H2O 6I2+12KOH+15O2↑
6I2+12KOH+15O2↑(第3小题第一小问2分,其它每空1分,共10分)
(1)检验母液中是否含有SO42-离子的方法是:取少量母液先加入稀盐酸酸化,再加入BaCl2溶液,若有白色沉淀,则说明有SO42-离子。
(2)过滤时,用到的玻璃仪器有:漏斗 玻璃棒 烧杯
(3)计算出1mL0.001mol/L KIO3中碘元素的质量,用碘元素质量除以精盐和KIO3的质量和,即可得到该碘盐的含碘量,约为25.4 mg/Kg,销售品≥30mg/Kg,所以此盐不合格。
(4)因为有碘单质生成,所以,还需要的一种试剂,最好是淀粉,因为碘遇淀粉变蓝色。
(5)碘酸钾两种情况下分解的化学方程式:2KIO3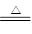 2KI+3O2↑ 12KIO3+6H2O
2KI+3O2↑ 12KIO3+6H2O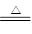 6I2+12KOH+15O2↑
6I2+12KOH+15O2↑
(2)过滤时,用到的玻璃仪器有:漏斗 玻璃棒 烧杯
(3)计算出1mL0.001mol/L KIO3中碘元素的质量,用碘元素质量除以精盐和KIO3的质量和,即可得到该碘盐的含碘量,约为25.4 mg/Kg,销售品≥30mg/Kg,所以此盐不合格。
(4)因为有碘单质生成,所以,还需要的一种试剂,最好是淀粉,因为碘遇淀粉变蓝色。
(5)碘酸钾两种情况下分解的化学方程式:2KIO3
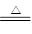 2KI+3O2↑ 12KIO3+6H2O
2KI+3O2↑ 12KIO3+6H2O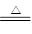 6I2+12KOH+15O2↑
6I2+12KOH+15O2↑
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
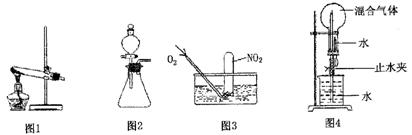


 根据硫化氢气体的实验室制法和性质完成下列填空。
根据硫化氢气体的实验室制法和性质完成下列填空。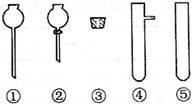
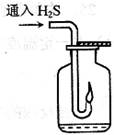

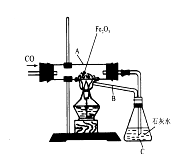
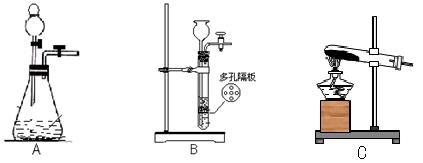
 ______________________,
______________________, 满的方法:____________________________________________________;
满的方法:____________________________________________________;