题目内容
同一物质往往可由不同化学反应途径制得,工业上往往主要考虑原料易得而丰富,工艺简单,污染小,经济效益好;实验室更多考虑药品常见易得,操作简便安全。你能想出多少种制备Al(OH)3的方法?写出有关反应原理的方程式,并从中优选一种简便方法,说明选择的理由。(至少列举四种)
(1)Al2(SO4)3+6NaOH ="===" 2Al(OH)3↓+3Na2SO4
(2)AlCl3+3NH3·H2O ="===" Al(OH)3↓+3NH4Cl
(3)3H2O+2KAl(SO4)2+3Na2CO3 ="===" K2SO4+3Na2SO4+2Al(OH)3↓+3CO2↑
(4)Al作阳极,Na2CO3作电解质溶液,电解:阳极:2Al-6e- ="===" 2Al3+
阴极:6H2O+6e- ="===" 3H2↑+6OH-
总反应方程式:2Al+6H2O 2Al(OH)3↓+3H2↑
2Al(OH)3↓+3H2↑
(5)Al2(SO4)3+6NH3·H2O====2Al(OH)3↓+3(NH4)2SO4
优选:(5),Al2(SO4)3性质稳定,是实验室常见药品,与NH3·H2O反应不会因碱的过量而使Al(OH)3溶解。
(2)AlCl3+3NH3·H2O ="===" Al(OH)3↓+3NH4Cl
(3)3H2O+2KAl(SO4)2+3Na2CO3 ="===" K2SO4+3Na2SO4+2Al(OH)3↓+3CO2↑
(4)Al作阳极,Na2CO3作电解质溶液,电解:阳极:2Al-6e- ="===" 2Al3+
阴极:6H2O+6e- ="===" 3H2↑+6OH-
总反应方程式:2Al+6H2O
 2Al(OH)3↓+3H2↑
2Al(OH)3↓+3H2↑(5)Al2(SO4)3+6NH3·H2O====2Al(OH)3↓+3(NH4)2SO4
优选:(5),Al2(SO4)3性质稳定,是实验室常见药品,与NH3·H2O反应不会因碱的过量而使Al(OH)3溶解。
AlCl3极易水解,在空气中吸湿水解挥发出HCl气体而“发烟”,难于保存;电解铝消耗大量电能,反应缓慢,现象不明显,需要仪器设备多,操作复杂。
其他合理答案只要方程式正确、说理合理,均可给分。
其他合理答案只要方程式正确、说理合理,均可给分。

练习册系列答案
相关题目
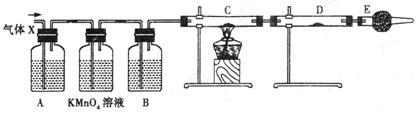
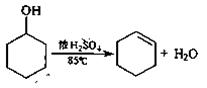
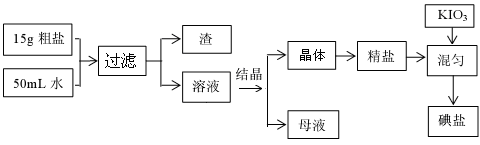
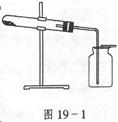
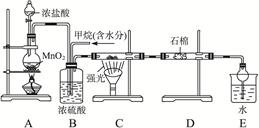 ?
?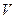 (Cl2)/
(Cl2)/ 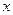 ,若理论上欲获得最多的氯化氢,则
,若理论上欲获得最多的氯化氢,则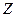 。
。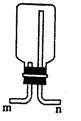
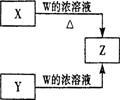
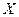 是黑色粉末,
是黑色粉末,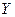 是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。
是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。