题目内容
用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A、8g甲烷含有的共价键数约为NA |
| B、常温常压下,22.4L二氧化碳原子总数为3NA |
| C、2.8g铁粉与足量稀硝酸反应,转移0.15NA个电子 |
D、 3.2g硫(结构见图)含S-S键的数目为0.8NA 3.2g硫(结构见图)含S-S键的数目为0.8NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.甲烷分子中含有4个碳氢共价键,8g甲烷的物质的量为0.5mol,含有2mol共价键;
B.常温常压下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量;
C.稀硝酸足量,铁反应生成了铁离子,2.8g铁的物质的量为0.05mol,完全反应失去0.15mol电子;
D.每个S原子与其它两个S形成了2个S-S共价键,根据均摊法计算出3.2gS形成的共价键数目.
B.常温常压下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量;
C.稀硝酸足量,铁反应生成了铁离子,2.8g铁的物质的量为0.05mol,完全反应失去0.15mol电子;
D.每个S原子与其它两个S形成了2个S-S共价键,根据均摊法计算出3.2gS形成的共价键数目.
解答:
解:A.8个甲烷的物质的量为0.5mol,0.5mol甲烷分子中含有2mol碳氢键,含有的共价键数约为2NA,故A错误;
B.常温下,不是标准状况下,题中条件无法计算22.4L二氧化碳的物质的量,故B错误;
C.2.8g铁粉的物质的量为0.05mol,与足量稀硝酸反应,0.05mol铁完全反应转移了0.15mol电子,转移0.15NA个电子,故C正确;
D.根据图示可知,每个S原子与其它两个S形成了2个S-S共价键,每个S形成的共价键数目为
×2=1,3.2gS的物质的量为0.1mol,形成了0.1molS-S共价键,0.1NA,故D错误;
故选C.
B.常温下,不是标准状况下,题中条件无法计算22.4L二氧化碳的物质的量,故B错误;
C.2.8g铁粉的物质的量为0.05mol,与足量稀硝酸反应,0.05mol铁完全反应转移了0.15mol电子,转移0.15NA个电子,故C正确;
D.根据图示可知,每个S原子与其它两个S形成了2个S-S共价键,每个S形成的共价键数目为
| 1 |
| 2 |
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项D为易错点,注意利用均摊法计算形成S-S键数目.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列选项的说法中正确的是( )
| A、分子的结构是由键角决定的 |
| B、共价键的键能越大,共价键越牢固 |
| C、CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 |
| D、H2O分子中的两个O-H键的键角为180° |
阿伏加德罗常数约为6.02×1023mol-1.下列叙述中正确的是( )
| A、32g含有少量臭氧的氧气中,共含有氧原子数为2×6.02×1023 |
B、32g S8单质中含有的S-S键个数为2NA(S8分子模型如图) |
| C、5.6g铁粉完全溶于硝酸,失去的电子数介于0.2×6.02×1023~0.3×6.02×1023之间 |
| D、在SiO2晶体中,若含有1mol Si原子,则含Si-O键数为2×6.02×1023 |
100mL Al2(SO4)3、K2SO4、KAl(SO4)2的混合液中,如果SO42-的浓度等于0.4mol/L,当加入2mol/L的KOH溶液50mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A、0.2mol?L-1 |
| B、0.05mol?L-1 |
| C、0.45mol?L-1 |
| D、0.225mol?L-1 |
下列说法不正确的是( )
| A、酸式滴定管、碱式滴定管、容量瓶、移液管都是准确量取一定体积液体的容器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 |
| B、纸层析法是以滤纸为惰性支持物,水为固定相,有机溶剂作流动相.用该方法可分离Fe3+和Cu2+,层析后氨熏显色,滤纸上方出现红棕色斑点 |
| C、进行分液操作时,应先打开上口活塞或使塞上的凹槽对准漏斗口的小孔,然后打开旋塞,下层液体从下口放出,上层液体从漏斗上口倒出 |
| D、在制备硝酸钾晶体的实验中,趁热过滤时,承接滤液的小烧杯中预先加2mL蒸馏水.以防过滤时氯化钠晶体析出 |
下列说法正确的是( )
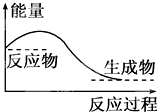

| A、任何化学反应都伴随着能量的变化 |
| B、H2O(g)═H2O(l)该过程放出大量的热,所以该过程是化学变化 |
| C、化学反应中能量的变化都表现为热量的变化 |
| D、对于如图所示的过程,是吸收能量的过程 |
对下列化学用语的理解和描述不正确的是( )
A、原子结构示意图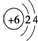 可以表示12C原子的,也可以表示14C原子的 可以表示12C原子的,也可以表示14C原子的 |
B、比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
C、结构示意图为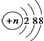 的阳离子都不能破坏水的电离平衡 的阳离子都不能破坏水的电离平衡 |
D、电子式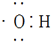 可以表示羟基,不可以表示氢氧根离子 可以表示羟基,不可以表示氢氧根离子 |
下列有关氕(H)、氘(D)、氚(T)的说法正确的是( )
| A、是三种不同的元素 |
| B、H元素平均的相对原子质量=(1+2+3)÷3 |
| C、通常我们把氢的相对原子质量当1来计算,这是以氕的相对原子质量为标准计算的 |
| D、自然界中所有含氢物质中都含有氕、氘、氚三种核素 |