题目内容
14.下列物质中既能脱水生成烯烃又能催化氧化生成醛的是( )| A. |  | B. |  | ||
| C. |  | D. |  |
分析 根据醇发生消去反应的结构特点是:与羟基所连碳相邻的碳上有氢原子才能发生消去反应,形成不饱和键;
醇发生氧化反应的结构特点是:有羟基所连碳上有氢原子的才能发生氧化反应,以此解答该题.
解答 解:A.可发生消去反应,不能发生催化氧化,故A错误;
B.可发生催化氧化生成醛,但不能发生消去反应,故B错误;
C.可以发生消去反应生成丙烯,发生氧化反应生成丙酮,故C错误;
D.既能发生消去反应生成烯烃,又能发生催化氧化反应生成醛,故D正确.
故选D.
点评 本题考查醇的消去反应、氧化反应,以及卤代烃的消去反应 难度不大,注意卤代烃发生消去反应的结构特点是:与-X相连碳相邻碳上有氢原子的才能发生消去反应.

练习册系列答案
相关题目
4.化学用语在化学学习中有着重要的作用.下列有关化学用语使用正确的是( )
| A. | CO2的电子式 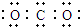 | B. | Cl-的结构示意图 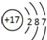 | ||
| C. | HCl的电子式 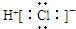 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |
5.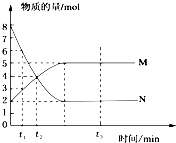 在一定温度下,将两种气体M和N通入容积为VL的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法正确的是( )
在一定温度下,将两种气体M和N通入容积为VL的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法正确的是( )
 在一定温度下,将两种气体M和N通入容积为VL的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法正确的是( )
在一定温度下,将两种气体M和N通入容积为VL的密闭容器中进行反应,M和N的物质的量与时间的关系如图所示,下列说法正确的是( )| A. | 0~t2内用M表示的平均反应速率是 $\frac{2}{{t}_{2}}$(mol•L-1•min-1) | |
| B. | t1~t2内容器内的压强逐渐减小 | |
| C. | 该反应的方程式为N?2M | |
| D. | t2与t3时刻的混合气体的平均相对分子质量相等 |
9.下列说法正确的是( )
| A. | 若完全燃烧,1 mol雌酮(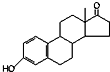 )比雄酮( )比雄酮(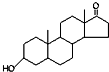 )多消耗3 mol O2 )多消耗3 mol O2 | |
| B. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| C. | 甲醛、甲酸、甲酸钠,均能发生银镜反应 | |
| D. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 |
19.下列属于极性分子的是( )
| A. | NH3 | B. | H2 | C. | CH4 | D. | BF3 |
6.下列说法不正确的是( )
①质子数相同的粒子一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎完全相同
③元素种类由质子数决定,原子种类由质子数和中子数共同决定,元素主要化学性质由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素.
①质子数相同的粒子一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎完全相同
③元素种类由质子数决定,原子种类由质子数和中子数共同决定,元素主要化学性质由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素.
| A. | ①②④⑤ | B. | ③④⑤ | C. | ②③⑤ | D. | ①⑤ |
3.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是( )
| A. | 由Al、Cu、稀H2SO4组成原电池,放电时SO42-向Al电极移动 | |
| B. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O | |
| C. | 由Al、Cu、浓硝酸组成原电池作电源,用石墨电极来电解硝酸银溶液,当析出1 mol Ag时,消耗铜电极32 g | |
| D. | 由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
4.下述实验设计合理的是( )
| A. | 用锌粒和稀硝酸反应制备H2 | B. | 用NH4NO3加热制取NH3 | ||
| C. | 大理石与稀硫酸反应制备CO2 | D. | 用焰色反应鉴别固体NaCl和 KCl |
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)