题目内容
19.下列属于极性分子的是( )| A. | NH3 | B. | H2 | C. | CH4 | D. | BF3 |
分析 极性分子中正负电荷的中心不重合,具有一定的极性,极性分子是由极性键构成的结构不对称的分子,以此解答该题.
解答 解:A.NH3中N原子形成3个δ键,有1个孤电子对,为sp3杂化,分子构型为三角锥形,空间结构不对称为极性分子,故A正确;
B.为非金属单质,只含有H-H键,为非极性分子,故B错误;
C.CH4为正四面体结构,为非极性分子,故C错误;
D.BF3分子中价层电子对个数=3+$\frac{1}{2}$×(5-3×1)=3且不含孤电子对,为平面三角形结构,为非极性分子,故D错误.
故选A.
点评 本题考查极性分子和非极性分子判断、原子杂化方式判断等知识点,侧重考查基本理论,难点是判断原子杂化方式,知道孤电子对个数的计算方法,为易错点.

练习册系列答案
相关题目
9.下列物质中可用作光导纤维的是( )
| A. | 单晶硅 | B. | 石英 | C. | 陶瓷 | D. | 水玻璃 |
10.由羟基与下列基团组成的化合物中,属于醇类的是( )
| A. | CH3CO- | B. |  | C. |  | D. | R-CO- |
7.下列说法正确的是( )
| A. | 明矾溶于水产生Al(OH)3 胶体,离子方程式可表示为:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 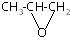 和CO2反应生成可降解聚合物 和CO2反应生成可降解聚合物 ,该反应符合绿色化学的原则 ,该反应符合绿色化学的原则 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 | |
| D. | 聚氯乙烯塑料制品可用于食品的包装 |
14.下列物质中既能脱水生成烯烃又能催化氧化生成醛的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
11.在反应:C+CO2 ?2CO中,可使反应速率增大的措施是( )
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤用等量炭粉代替焦炭.
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤用等量炭粉代替焦炭.
| A. | ①②③ | B. | ②③④⑤ | C. | ①②③⑤ | D. | ②③④ |
9.用图中装置进行实验,实验一段时间后,现象与预测不一致的是( )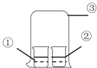

| ①中物质 | ②中物质 | 实验预测 | |
| A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
| B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
| C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
| D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
| A. | A | B. | B | C. | C | D. | D |
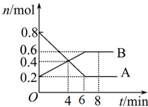 某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.
某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示.